- Verfügbarkeit: Auf Lager
- Package: 1mg/vial+water
Stellen Sie eine Frage zu diesem Produkt
Longes Arginin 3-IGF-1, abgekürzt als IGF-1 LR3 oder LR3-IGF-1, ist ein synthetisches Protein und verlängertes Analogon des menschlichen insulinähnlichen Wachstumsfaktors 1 (IGF-1).
WAS IST IGF-1?
Insulinähnlicher Wachstumsfaktor 1 (IGF-1) ist ein lebenswichtiges Protein, das eine zentrale Rolle im menschlichen Wachstum und in der Entwicklung spielt. Dieses rekombinante menschliche Protein, das zur Familie der insulinähnlichen Wachstumsfaktoren gehört, besteht aus 70 Aminosäuren und funktioniert ähnlich wie Insulin. Es ist an der Regulierung verschiedener Körperprozesse beteiligt, einschließlich Zellwachstum, -entwicklung und -differenzierung, durch endokrine, autokrine und parakrine Wege.
Einer der interessanten Aspekte von IGF-1 ist seine Verbindung zum Altern. Forschungen deuten darauf hin, dass Mutationen im IGF-1-Gen die Lebensdauer von Labortieren verlängern können, was seine potenzielle Wirkung auf die Langlebigkeit hervorhebt. Bei Kindern ist IGF-1 entscheidend für die Stimulation von Zellwachstum und -differenzierung, während es bei Erwachsenen weiterhin anabole Effekte ausübt und das Wachstum und die Erhaltung des Gewebes fördert.
IGF-1 operiert innerhalb eines komplexen Netzwerks von Wachstumsfaktoren, Rezeptoren und Bindungsproteinen, die die Zellproliferation, -differenzierung und Apoptose vermitteln. Diese Wachstumsfaktoren sind niedermolekulare Proteine, die in fast allen Geweben vorkommen und dort die Zellteilung, das Wachstum und die Migration regulieren. In der Haut sind sie beispielsweise entscheidend für die Migration und Entwicklung von Epithelzellen und stimulieren die Zellteilung.
Oft als Somatomedin C bezeichnet, dient IGF-1 als Schlüsselmediator der Wirkungen des Wachstumshormons (HGH). Es wird hauptsächlich von Leber-Hepatozyten als Reaktion auf die Stimulation durch Wachstumshormon produziert. Die Produktion von IGF-1 in der Leber wird von verschiedenen Hormonen beeinflusst, darunter Sexualsteroide, Schilddrüsenhormone, Glukokortikoide und Insulin. Insulin, Androgene und Östrogene neigen dazu, die IGF-1-Sekretion zu erhöhen, während Glukokortikoide sie hemmen. Dieses Zusammenspiel erklärt die Synergie zwischen diesen Hormonen in Wachstums- und Entwicklungsprozessen und die hemmende Wirkung von Glukokortikoiden auf Wachstum und Pubertät.
Im Laufe des Lebens schwanken die IGF-1-Spiegel, sie erreichen ihren Höhepunkt während der Adoleszenz und sinken in der Kindheit und im Alter. Trotz dieser Schwankungen bleibt IGF-1 ein wichtiges anaboles Hormon. Es wird von verschiedenen Geweben sezerniert, wobei die Leber die Hauptquelle darstellt, die IGF-1 in den Blutkreislauf freisetzt, um als endokrines Hormon zu wirken. Andere Gewebe, einschließlich Knorpelzellen, sezernieren ebenfalls IGF-1, wo es lokal als parakrines Hormon wirkt.
In den letzten Jahren hat IGF-1 in der Sportwelt als Dopingmittel Aufmerksamkeit erregt und war in zahlreichen hochkarätigen Dopingfällen involviert. Seine Fähigkeit, Wachstum und Leistung zu steigern, macht es zu einem Stoff von Interesse und Besorgnis in der Athletengemeinschaft.
WAS IST DER UNTERSCHIED ZWISCHEN IGF-1 UND IGF-1 LR3?
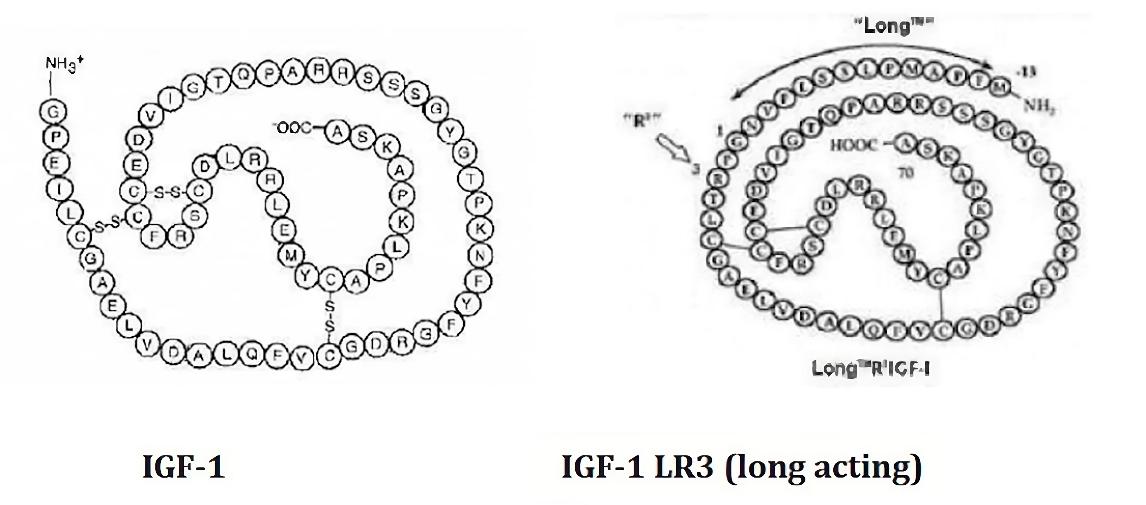
Der insulinähnliche Wachstumsfaktor 1 (IGF-1) und seine erweiterte Variante, IGF-1 LR3, weisen viele Gemeinsamkeiten auf, aber auch deutliche Unterschiede, die ihre Funktionen und Anwendungen beeinflussen. IGF-1 ist ein natürlich vorkommendes Protein im menschlichen Körper, das für Zellwachstum, -entwicklung und -differenzierung entscheidend ist. Es besteht aus 70 Aminosäuren und wirkt, indem es an IGF-1-Rezeptoren bindet und verschiedene physiologische Prozesse beeinflusst.
IGF-1 LR3 hingegen ist eine modifizierte Form von IGF-1, die so konstruiert wurde, dass sie eine längere Halbwertszeit und eine erhöhte Stabilität aufweist. Diese Variante enthält 13 zusätzliche Aminosäuren am N-Terminus, wobei die ursprüngliche dritte Aminosäure, Glutaminsäure, durch Arginin ersetzt wurde. Diese Modifikation reduziert die Bindungsaffinität von IGF-1 LR3 zu IGF-Bindungsproteinen erheblich, die normalerweise die Verfügbarkeit und Aktivität von IGF-1 regulieren. Dadurch bleibt IGF-1 LR3 länger im Blutkreislauf aktiv, was seine Wirksamkeit bei der Förderung von Wachstum und anabolen Prozessen erhöht.
Die verlängerte Halbwertszeit von IGF-1 LR3 macht es sowohl in medizinischen als auch in sportlichen Kontexten besonders wertvoll. In medizinischen Bereichen bietet es potenzielle therapeutische Vorteile bei Erkrankungen, die eine verlängerte IGF-1-Aktivität erfordern, wie z. B. Muskelschwund und Wachstumsstörungen. Im Sport und Bodybuilding ist seine verlängerte Wirkung und seine starken anabolen Effekte ein begehrter Wirkstoff zur Förderung des Muskelwachstums und der Leistung. Dies wirft jedoch auch Bedenken hinsichtlich seines Missbrauchs und der ethischen Implikationen im Leistungssport auf.
Zusammenfassend lässt sich sagen, dass sowohl IGF-1 als auch IGF-1 LR3 wichtige Rollen im Wachstum und in der Entwicklung spielen, wobei der entscheidende Unterschied in der konstruierten Struktur von IGF-1 LR3 liegt, die ihm eine längere Halbwertszeit und eine höhere Wirksamkeit verleiht. Diese Unterscheidung erweitert nicht nur seine potenziellen therapeutischen Anwendungen, sondern unterstreicht auch die Notwendigkeit einer sorgfältigen Regulierung, um Missbrauch im sportlichen Umfeld zu verhindern.
HAUPTEFFEKTE
IGF-1 ist ein äußerst starkes anaboles Mittel, das in Kombination mit anabolen Steroiden zu einem sehr großen Zuwachs an fettfreier Muskelmasse führt. Gleichzeitig hat IGF-1 viele andere nützliche Eigenschaften, die zusammen das maximale Wachstumspotenzial schaffen. IGF-1 ist ein Produkt, das Ihre Ergebnisse steigern kann, wenn andere Methoden keine signifikanten Effekte mehr erzielen.
Anabole Effekte
- Zunahme der Muskelmasse (verschiedene Arten der Exposition)
- Muskelhyperplasie (einzigartige Eigenschaft, die Anzahl der Muskelzellen zu erhöhen)
- Beschleunigte Proteinsynthese
- Regeneration des Sehnengewebes (erhöht die Kollagensynthese)
- Hat eine regenerierende Wirkung auf Knorpelgewebe
- Erhöht die Wirksamkeit anaboler Steroide (erhöht die Anzahl der Androgenrezeptoren)
- Stellt Knochen- und Knorpelgewebe wieder her und stärkt es
Unterstützung des Herz-Kreislauf-Systems
- Verbessert das Herzzeitvolumen, Schlagvolumen, Kontraktilität und die Ejektionsfraktion.
- Stimuliert die Kontraktilität und das Gewebereparatur bei Menschen, um die Herzfunktion nach einem Myokardinfarkt zu verbessern.
- Verbessert das Lipidprofil
- Reduziert Insulinspiegel, erhöht die Insulinsensitivität und fördert den Glukosestoffwechsel
- Reduziert das allgemeine Risiko kardiovaskulärer Komplikationen
- Hilft, entzündliche Prozesse zu bekämpfen
Nervengewebe
- Erhöht den Glukosetransport im Nervengewebe
- Schützt Neuronen bei niedrigen Glukosespiegeln, verhindert Zellzerstörung.
- Spielt eine wichtige Rolle bei der Wiederherstellung von Neuronen und Nervengewebe im Allgemeinen
Weitere Effekte
- Regulieren die Expression von Genen, die die Lebenserwartung erhöhen.
- Beschleunigt die Hautregeneration, verhindert Hautalterung
- Verbesserte Immunität
Wirkmechanismus
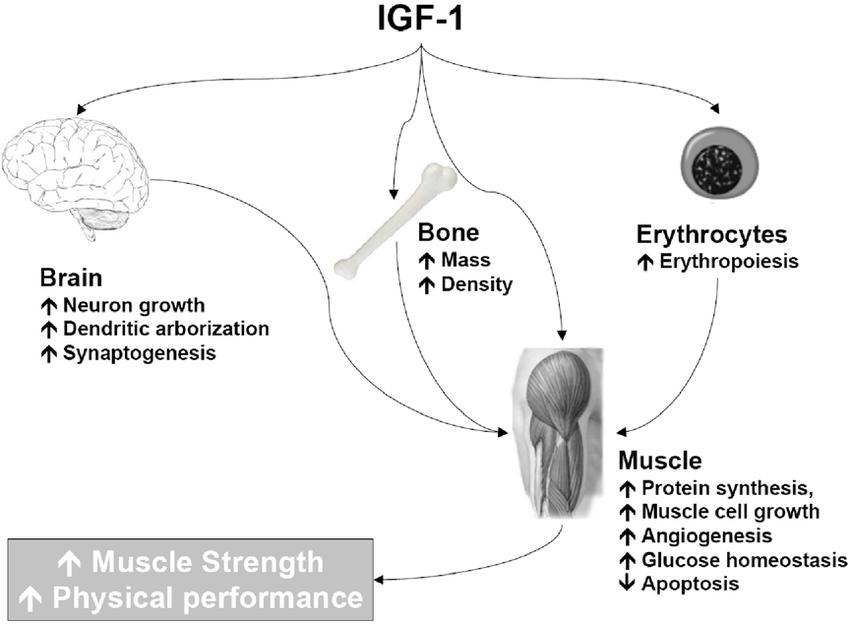
Insulinähnlicher Wachstumsfaktor 1 (IGF-1) ist ein lebenswichtiges Protein, das eine entscheidende Rolle bei der Regeneration und Reparatur verschiedener Gewebe im menschlichen Körper spielt, einschließlich Knochen, Muskeln, Haut und Knorpel. Wenn IGF-1 mit Knochen- und Knorpelgewebe interagiert, bindet es sich an spezifische Rezeptoren auf Osteoblasten und Chondroblasten—Zellen, die für das Wachstum und die Reparatur von Knochen und Knorpel verantwortlich sind. Diese Bindung stimuliert die Stoffwechselaktivität dieser Zellen, was zu einer beschleunigten Heilung von Brüchen und anderen Knochenverletzungen führt. IGF-1 reduziert auch Entzündungen in den beschädigten Bereichen und erhöht die Aktivität der Zellen, die an der Gewebserneuerung beteiligt sind (Yakar et al., 2019).
Darüber hinaus gehen die metabolischen Effekte von IGF-1 über Wachstum und Reparatur hinaus. Es spielt eine bedeutende Rolle bei der Nährstoffsignalisierung, indem es den Protein-, Fett- und Kohlenhydratstoffwechsel über verschiedene Zelltypen hinweg koordiniert. Dies wird durch die Stimulation der IGF-1-Rezeptoren erreicht, die den Zellen signalisieren, welche Nährstoffe verfügbar sind. Diese Koordination sorgt dafür, dass die Zellen die notwendigen Nährstoffe für Wachstum und Erhalt erhalten. Wie Insulin wird IGF-1 durch den Ernährungsstatus reguliert und spielt eine Rolle bei der Glukosehomöostase. Es senkt den Blutzuckerspiegel, indem es die Glukoseaufnahme in den Zellen erhöht und die Insulinsekretion reduziert, was die Insulinsensitivität verbessert (Samani et al., 2007).
Neben seiner Rolle im Stoffwechsel beeinflusst IGF-1 auch den Proteinmetabolismus und die Lipolyse. Es wirkt synergetisch mit Wachstumshormon (GH), um den Fettabbau zu fördern und die Ketogenese zu unterstützen. Diese Synergie zwischen IGF-1 und GH ist entscheidend für die Aufrechterhaltung des Energiegleichgewichts und die Unterstützung von Wachstumsprozessen. Studien haben gezeigt, dass niedrige IGF-1-Spiegel häufig mit dem metabolischen Syndrom verbunden sind, einem Cluster von Bedingungen, die das Risiko für Herzerkrankungen, Schlaganfälle und Diabetes erhöhen. Dies unterstreicht die Bedeutung von IGF-1 für die Aufrechterhaltung der allgemeinen metabolischen Gesundheit (Clemmons, 2004).
Effekte auf Muskeln
IGF-1 hat einen tiefgreifenden Einfluss auf das Muskelgewebe, indem es das Muskelwachstum und die Muskelreparatur fördert. Dies wird hauptsächlich durch die Stimulation von Satellitenzellen erreicht, die Stammzellen im Muskelgewebe sind. Wenn Muskelgewebe beschädigt wird, aktiviert IGF-1 diese Satellitenzellen, wodurch sie sich vermehren und zu neuen Muskelzellen differenzieren. Dieser Prozess repariert nicht nur beschädigte Muskelfasern, sondern führt auch zu einer Zunahme der Muskelmasse. Die Fähigkeit von IGF-1, die Muskelregeneration zu verbessern, macht es zu einer wichtigen Behandlung bei Zuständen, die mit Muskelatrophie einhergehen, wie z. B. Muskeldystrophie (Ahmad et al., 2020).
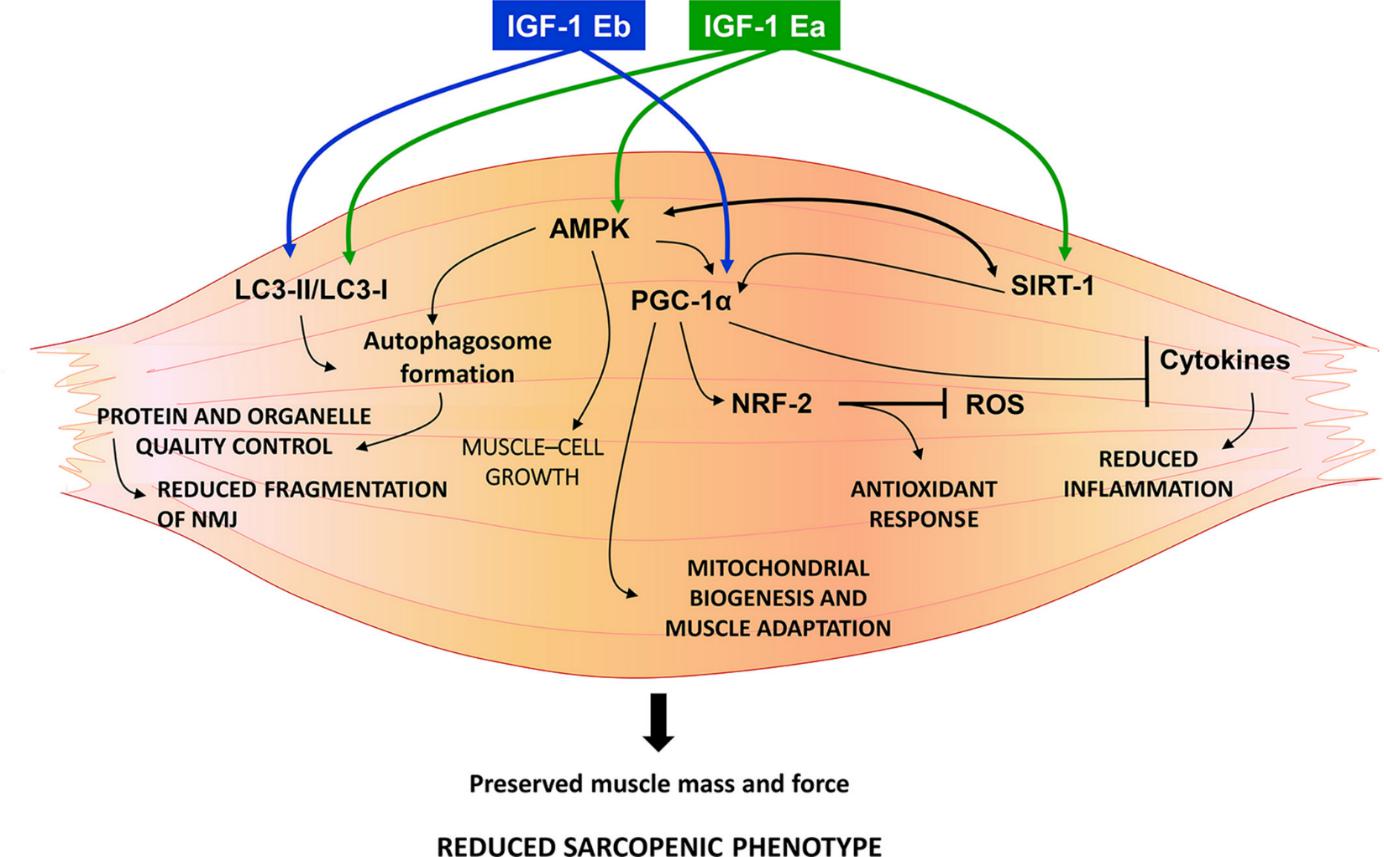
Die molekularen Mechanismen, durch die IGF-1 das Muskelwachstum stimuliert, umfassen mehrere Signalwege. Einer der Hauptwege ist der PI-3-Kinase-Weg, der zur Aktivierung der Proteinkinase B (AKT) führt. AKT fördert dann die Proteinsynthese, indem es den mTOR-Weg aktiviert, einen entscheidenden Regulator des Zellwachstums und der Proteinsynthese. Darüber hinaus verbessert IGF-1 den Transport von Aminosäuren in Muskelzellen, wodurch die notwendigen Bausteine für die Proteinsynthese bereitgestellt werden. IGF-1 hemmt auch den Proteinabbau, indem es die Expression von Genen herunterreguliert, die an Muskelatrophie beteiligt sind, wie MuRF1 und MAFbx (Lai et al., 2004).
Neben seinen anabolen Effekten hat IGF-1 auch anti-katabolische Eigenschaften. Es wirkt den Effekten entzündlicher Zytokine entgegen, die den Muskelabbau fördern. Durch die Hemmung dieser katabolischen Wege hilft IGF-1, die Muskelmasse und -funktion zu erhalten, selbst unter Stressbedingungen oder bei Krankheiten. Diese doppelte Rolle bei der Förderung des Muskelwachstums und der Verhinderung des Muskelabbaus macht IGF-1 zu einem wesentlichen Faktor für die Aufrechterhaltung der Muskelgesundheit und -funktion (Lai et al., 2004).
Effekte auf Sehnengewebe
Sehnenverletzungen heilen notorisch langsam und führen oft zu fibro-vaskulären Narben, die die mechanischen Eigenschaften der Sehnen beeinträchtigen und das Risiko einer erneuten Verletzung erhöhen. Es hat sich gezeigt, dass IGF-1 die Sehnenheilung erheblich verbessert, indem es die Zellproliferation, DNA-Synthese und Matrixproduktion, insbesondere Kollagen I, das Hauptbestandteil des Sehnengewebes ist, fördert. Dies macht IGF-1 zu einem starken anabolen Mittel zur Verbesserung der Sehnenreparatur und -funktion (Miescher et al., 2023).
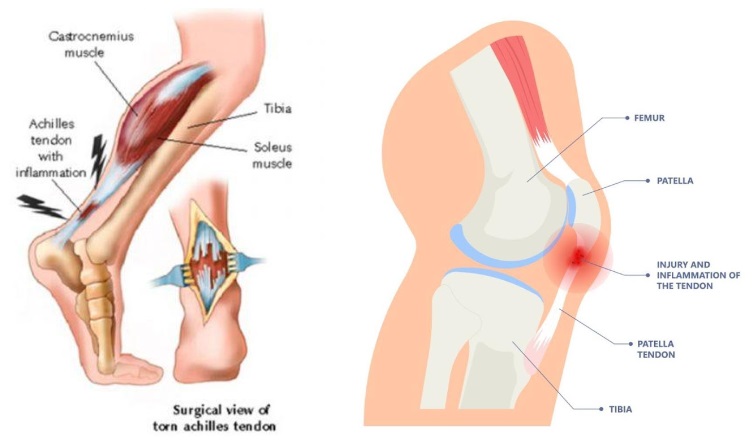
Der Mechanismus, durch den IGF-1 die Sehnenheilung fördert, umfasst mehrere zelluläre Prozesse. Wenn IGF-1 auf Tenozytenkulturen – Zellen, die die Sehnen bilden – angewendet wird, stimuliert es diese Zellen zur Proliferation und zur Produktion von mehr Bestandteilen der extrazellulären Matrix, einschließlich Kollagen. Diese verstärkte Matrixproduktion bietet die strukturelle Unterstützung, die für die Sehnenreparatur erforderlich ist. Zusätzlich wurde gezeigt, dass IGF-1 die Entzündung in der verletzten Sehne reduziert, was den Heilungsprozess weiter unterstützt, indem es ein günstigeres Umfeld für die Geweberegeneration schafft (Disser et al., 2019).
In präklinischen Tiermodellen und bei menschlichen Patienten hat IGF-1 seine Wirksamkeit bei der Verbesserung der Sehnenheilungsergebnisse gezeigt. Studien haben beispielsweise gezeigt, dass die Anwendung von IGF-1 auf verletzte Sehnen in Tiermodellen den Heilungsprozess beschleunigt, Narbenbildung reduziert und die mechanischen Eigenschaften der geheilten Sehnen verbessert. Diese Ergebnisse deuten darauf hin, dass IGF-1 ein wertvolles Therapeutikum für die Behandlung von Sehnenverletzungen in klinischen Umgebungen sein könnte (Doessing et al., 2010).
Wirkungen auf das Knorpelgewebe
IGF-1 spielt eine entscheidende Rolle bei der Erhaltung und Reparatur von Knorpelgewebe, das für die Gesundheit und Funktion der Gelenke unerlässlich ist. Knorpel ist ein widerstandsfähiges und glattes elastisches Gewebe, das die Enden der langen Knochen an den Gelenken bedeckt und schützt. Es dient auch als Polster zwischen den Knochen und ermöglicht eine reibungslose und schmerzfreie Bewegung. IGF-1 reguliert den Knorpelstoffwechsel, indem es anabole Prozesse fördert und katabole Prozesse hemmt, wodurch die Integrität und Funktion des Knorpels aufrechterhalten werden (Wen et al., 2021).
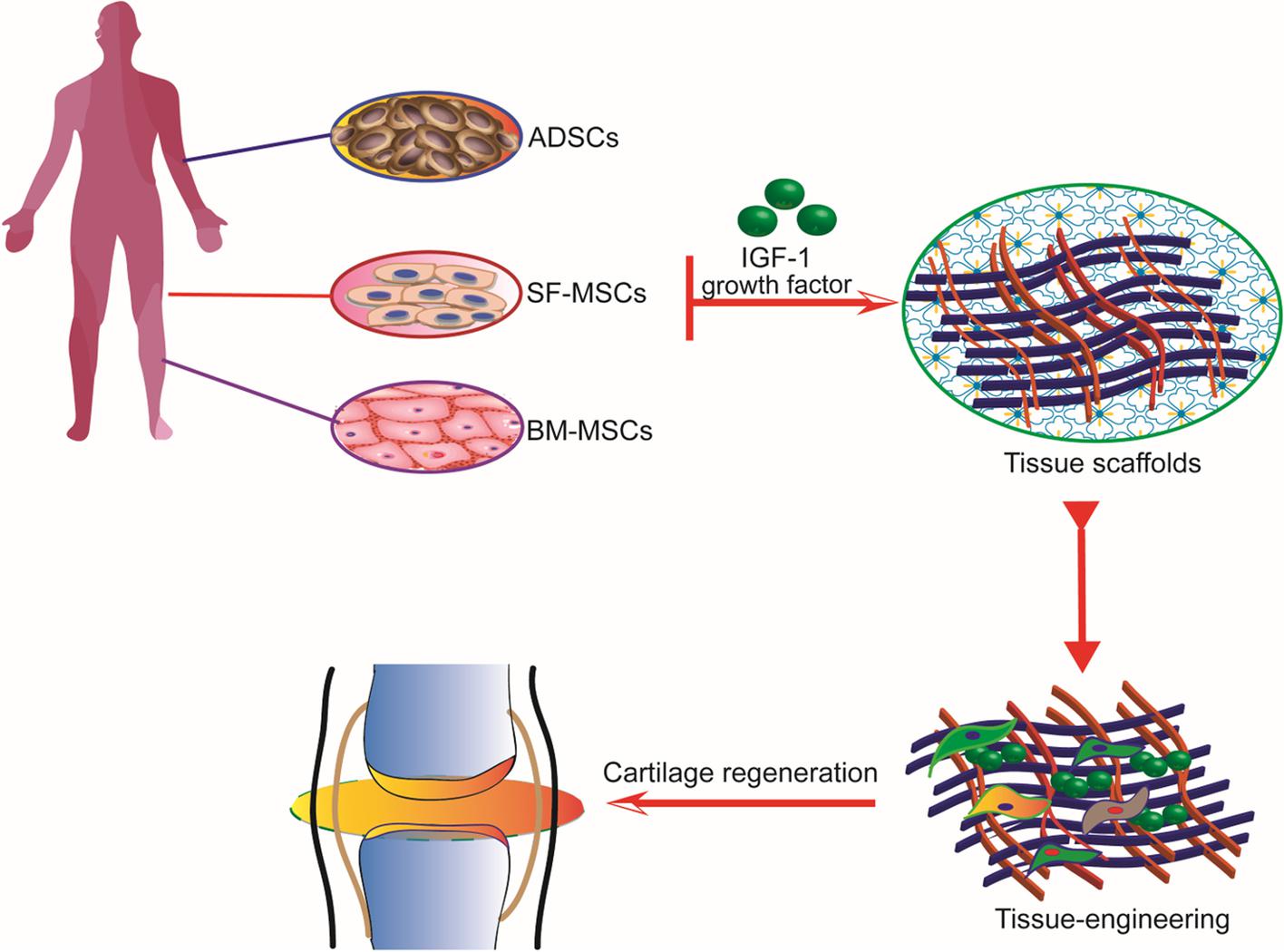
Die primären Zellen, die für die Erhaltung des Knorpels verantwortlich sind, sind Chondrozyten. IGF-1 stimuliert diese Zellen zur Produktion von Bestandteilen der extrazellulären Matrix, wie Kollagen und Proteoglykane, die für die Struktur und Funktion des Knorpels unerlässlich sind. Zusätzlich zur Förderung der Matrixsynthese hemmt IGF-1 die Aktivität von Enzymen, die den Knorpel abbauen, wie Matrix-Metalloproteinasen (MMPs). Diese doppelte Wirkung, anabole Prozesse zu fördern und katabole Prozesse zu hemmen, hilft, das Knorpelgewebe zu erhalten und eine Degeneration zu verhindern (Vedadghavami, 2022).
Studien haben gezeigt, dass IGF-1 das Fortschreiten der Osteoarthritis, einer degenerativen Gelenkerkrankung, die durch den Abbau von Knorpel gekennzeichnet ist, verlangsamen kann. Eine effektive Verabreichung von IGF-1 an beschädigten Knorpel ist entscheidend für seine therapeutischen Wirkungen. Techniken wie intraartikuläre Injektionen und lokalisierte Abgabesysteme werden untersucht, um sicherzustellen, dass IGF-1 das Zielgewebe in ausreichenden Konzentrationen erreicht. Tierstudien haben gezeigt, dass die kontinuierliche Verabreichung von IGF-1 den Knorpelabbau verhindern und die Reparatur fördern kann, was sein Potenzial als Behandlung für Osteoarthritis hervorhebt (Wen et al., 2021).
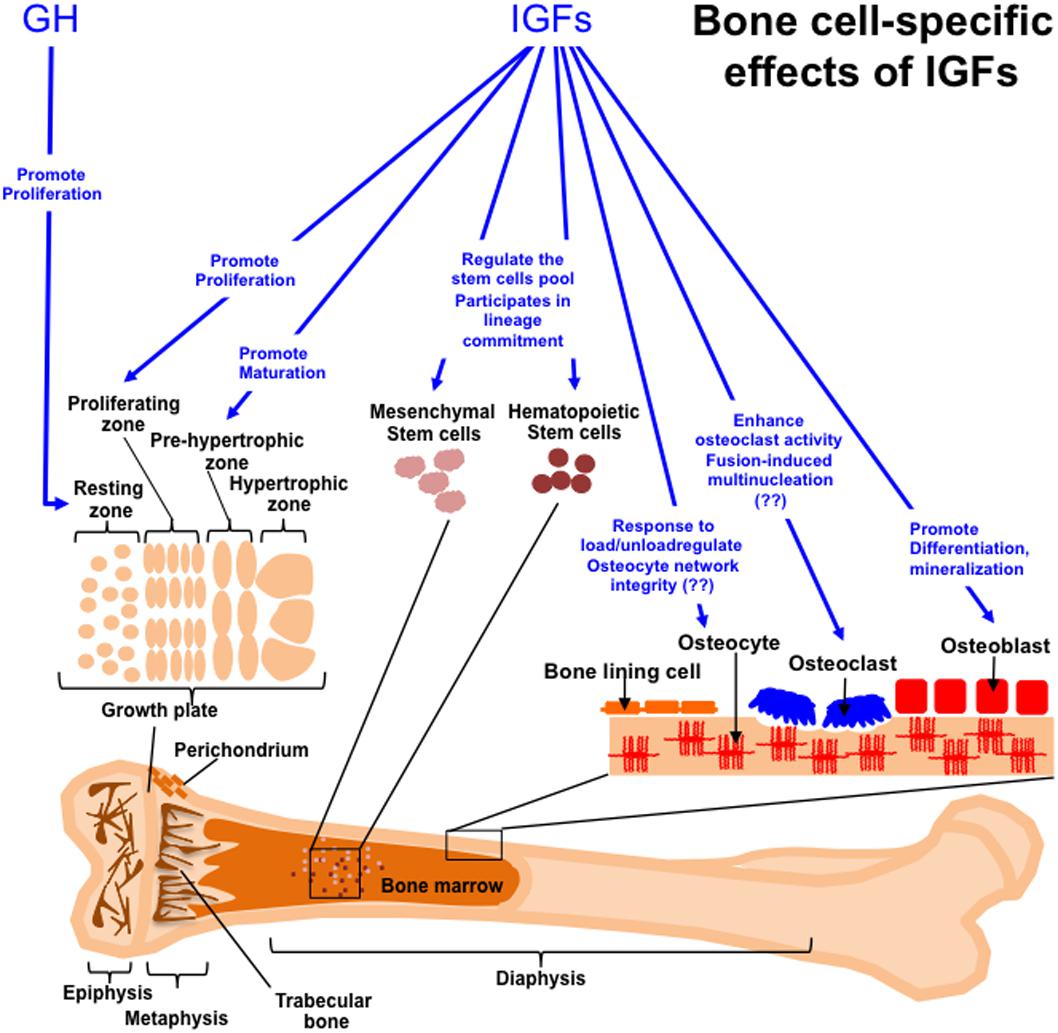
Knochengewebe
IGF-1 beeinflusst den Knochenstoffwechsel erheblich, indem es sowohl den Knochenabbau als auch die Knochenbildung fördert. Diese doppelte Wirkung ist entscheidend für das Knochenumbau, einen kontinuierlichen Prozess, bei dem altes Knochengewebe durch neues ersetzt wird. IGF-1 stimuliert Osteoblasten, die Zellen, die für die Knochenbildung verantwortlich sind, zur Produktion neuer Knochenmatrix. Es fördert auch die Aktivität von Osteoklasten, den Zellen, die für den Knochenabbau verantwortlich sind, um altes oder beschädigtes Knochengewebe zu entfernen und den Ersetzungsprozess zu erleichtern (Canalis, 2009).
Die Wirkungen von IGF-1 auf die Knochengesundheit sind besonders deutlich bei Zuständen, die Knochenbrüche und Osteoporose betreffen. Studien haben gezeigt, dass die Verabreichung von IGF-1 an Patienten mit Knochenbrüchen die Knochenheilung beschleunigen und die klinischen Ergebnisse verbessern kann. Beispielsweise wurde festgestellt, dass die IGF-1-Behandlung die Knochendichte erhöht und die strukturellen Eigenschaften des geheilten Knochens verbessert, wodurch er stärker und weniger anfällig für erneute Verletzungen wird (Locatelli & Bianchi., 2014).
Zusätzlich zu seinen direkten Wirkungen auf Knochenzellen beeinflusst IGF-1 auch die Knochengesundheit, indem es mit anderen Hormonen wie dem Parathormon (PTH) und Vitamin D interagiert. Diese Wechselwirkungen helfen, den Kalziumhaushalt zu regulieren und sicherzustellen, dass die Knochen ausreichend Nährstoffe für Wachstum und Reparatur erhalten. Durch die Modulation dieser hormonellen Wege spielt IGF-1 eine entscheidende Rolle bei der Erhaltung der Knochengesundheit und der Vorbeugung von Krankheiten wie Osteoporose (Canalis, 2010).
IGF-1 und Glukosestoffwechsel
IGF-1 hat signifikante Auswirkungen auf den Glukosestoffwechsel, insbesondere auf die Verbesserung der Insulinsensitivität und die Regulierung des Blutzuckerspiegels. Es stimuliert den Glukosetransport in Muskelzellen durch IGF-1-Rezeptoren oder hybride Insulin/IGF-1-Rezeptoren. Durch die Erhöhung der Glukoseaufnahme in Muskelzellen hilft IGF-1, den Blutzuckerspiegel zu senken, wodurch der Bedarf an Insulinsekretion reduziert wird (Clemmons, 2004).
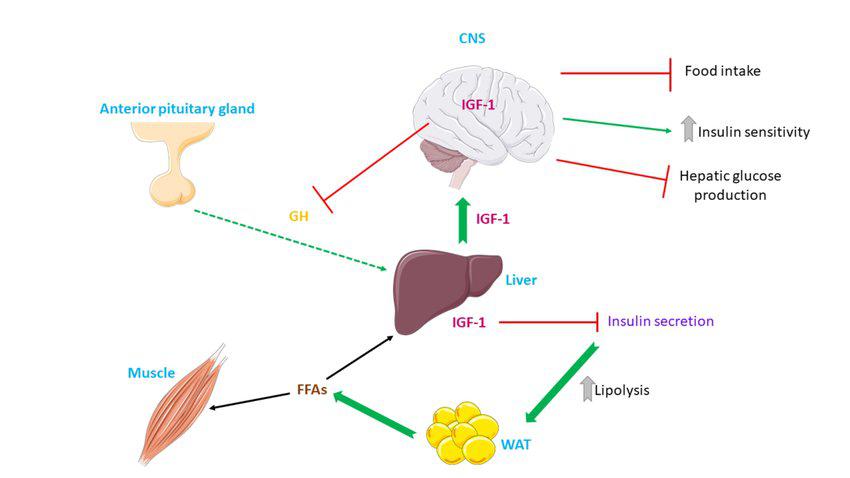
Beschreibung der durch IGF-1 hervorgerufenen metabolischen Wirkungen. IGF-1 wird hauptsächlich von der Leber freigesetzt und verbessert die Insulinsensitivität durch Unterdrückung der Insulinsekretion, was wiederum zu einer verstärkten Lipolyse im Fettgewebe und einer Förderung der NEFA-Nutzung in Muskeln und Leber führt. Abkürzungen verwendet: ZNS: zentrales Nervensystem; GH: Wachstumshormon; IGF-1: Insulinähnlicher Wachstumsfaktor-1; FFAs: freie Fettsäuren; WAT: weißes Fettgewebe.
In Tiermodellen wurde gezeigt, dass hohe Konzentrationen von freiem IGF-1 die Glukoneogenese hemmen, den Prozess, durch den Glukose aus nicht-kohlenhydrathaltigen Quellen in der Leber produziert wird. Diese Hemmung hilft, den Blutzuckerspiegel zu senken und verbessert das allgemeine Glukosegleichgewicht. Darüber hinaus haben Studien gezeigt, dass die Entfernung des Insulinrezeptors bei Mäusen den Blutzuckerspiegel als Reaktion auf IGF-1 senkt, was darauf hinweist, dass IGF-1 die Rolle von Insulin im Glukosestoffwechsel bis zu einem gewissen Grad kompensieren kann (Clemmons, 2004).
Klinische Studien haben ebenfalls die Bedeutung von IGF-1 für die Aufrechterhaltung des Glukosestoffwechsels hervorgehoben. Zum Beispiel haben Forschungen gezeigt, dass niedrige Serum-IGF-1-Spiegel mit gestörter Glukosetoleranz und einem erhöhten Risiko für Typ-2-Diabetes verbunden sind. Umgekehrt korrelieren höhere IGF-1-Spiegel mit besserer Insulinsensitivität und niedrigeren Blutzuckerspiegeln. Diese Ergebnisse deuten darauf hin, dass IGF-1 eine entscheidende Rolle bei der Prävention von Stoffwechselstörungen und der Aufrechterhaltung des Glukosegleichgewichts spielt (Rajpathak et al., 2014).
IGF-1 und Altern
Der IGF-1-Weg ist hochgradig konserviert bei verschiedenen Spezies, von Wirbellosen bis zu Säugetieren. Dieser Weg ist entscheidend für die Regulierung von Wachstum, Entwicklung und Lebensdauer. Bei Säugetieren umfasst der IGF-1-Weg ein komplexes Netzwerk von Signalen, die zelluläre Prozesse wie Wachstum, Stoffwechsel und Altern beeinflussen. IGF-1 übt seine Wirkungen über den IGF-1-Rezeptor aus, der eine Kaskade von intrazellulären Signalwegen aktiviert, die das Zellwachstum und Überleben fördern (Kenyon, 2010).
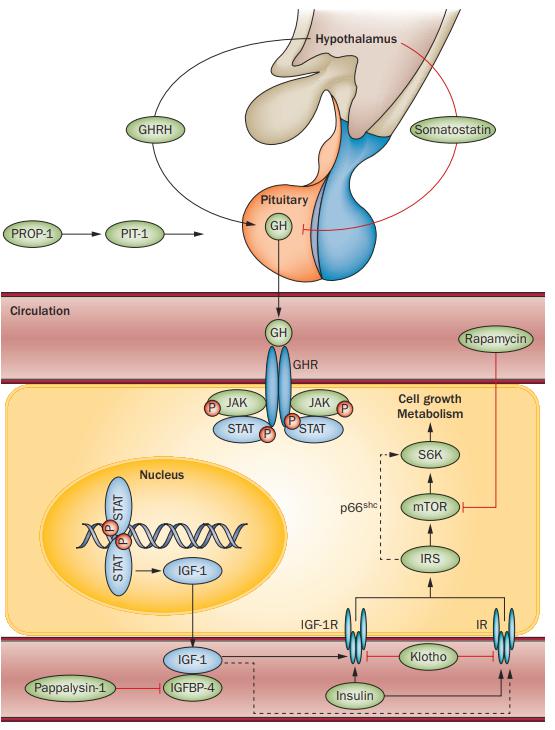
Faktoren der GH/IGF-1-Achse, die das Altern beeinflussen. Die embryonal exprimierten Gene PROP1 (das für PROP-1 kodiert) und POU1F1 (das für PIT-1 kodiert) sind an der Entwicklung der Hypophyse beteiligt, einschließlich der Differenzierung der somatotrophen Zellen der Hypophyse.
Während es bei Wirbellosen einen einzigen Insulin/IGF-1-Weg gibt, ist dieser Weg bei höheren Wirbeltieren, einschließlich Säugetieren, in zwei Teile aufgeteilt. Diese beiden Wege haben überlappende Funktionen, aber Insulin ist hauptsächlich an der Regulierung des Stoffwechsels beteiligt, während der Wachstumshormon/IGF-1-Weg eine wichtige Rolle bei Wachstums-, Entwicklungsprozessen und möglicherweise bei der Lebenserwartung spielt. Es waren die IGF-1-Kaskadengene, die als erste entdeckte „Altersgene“ identifiziert wurden – das heißt, Gene, deren Schädigung zu einer Verlängerung der Lebenserwartung führte.
Beim Menschen wurden Variationen in den IGF-1-Spiegeln und Signalwegen mit altersbedingten Krankheiten in Verbindung gebracht. Niedrige IGF-1-Spiegel sind oft mit einem erhöhten Risiko für Herz-Kreislauf-Erkrankungen, Diabetes und neurodegenerative Störungen verbunden. Umgekehrt werden höhere IGF-1-Spiegel mit besseren Gesundheitsergebnissen und einem geringeren Risiko für diese Erkrankungen in Verbindung gebracht. Diese Ergebnisse unterstreichen die Bedeutung von IGF-1 bei der Förderung eines gesunden Alterns und der Prävention altersbedingter Krankheiten (Kenyon, 2010).
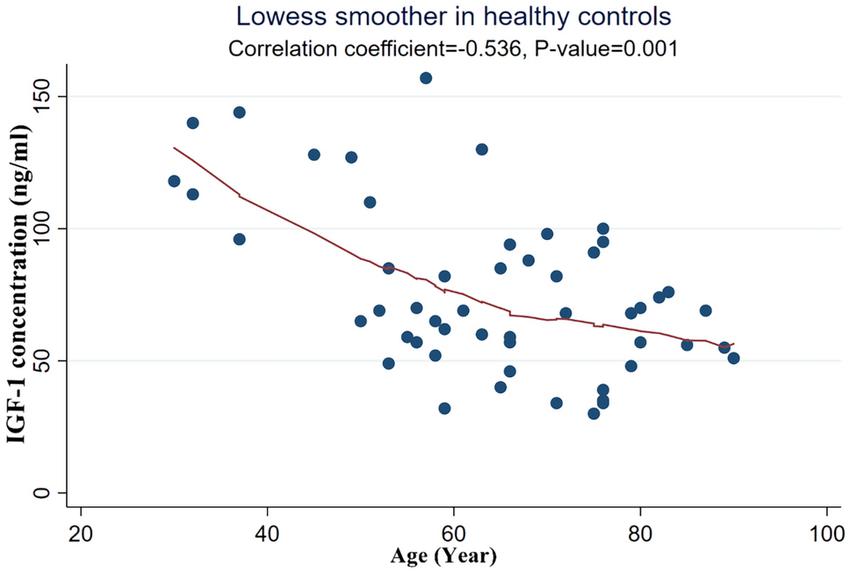
Wirkungen auf die Haut
IGF-1 spielt eine entscheidende Rolle bei der Erhaltung der Hautgesundheit und der Förderung der Wundheilung. Es wirkt als Regulator und Stimulator der Zellteilung im Epithelgewebe und fördert das Wachstum und den Stoffwechsel von Zellen in den tieferen Hautschichten. Dies führt zu einer beschleunigten Kollagensynthese und einer schnelleren Heilung sowohl oberflächlicher als auch tiefer Wunden. IGF-1 spielt auch eine Schlüsselrolle bei der Aufrechterhaltung der epidermalen Homöostase, was dazu beiträgt, Hautalterung zu verhindern und ein jugendliches Aussehen zu bewahren (Tavakkol et al., 1999).
Der Mechanismus, durch den IGF-1 die Hautgesundheit fördert, umfasst mehrere zelluläre Prozesse. Bei Hautverletzungen stimuliert IGF-1 die Proliferation von Keratinozyten, den Hauptzellen der Epidermis, und Fibroblasten, den Zellen, die für die Produktion von Kollagen und anderen Bestandteilen der extrazellulären Matrix verantwortlich sind. Diese erhöhte Zellproliferation und Matrixproduktion hilft, die beschädigte Haut zu reparieren und ihre strukturelle Integrität wiederherzustellen. Zusätzlich fördert IGF-1 die Migration dieser Zellen zur Wundstelle, was den Heilungsprozess weiter beschleunigt (Zhang et al., 2024).
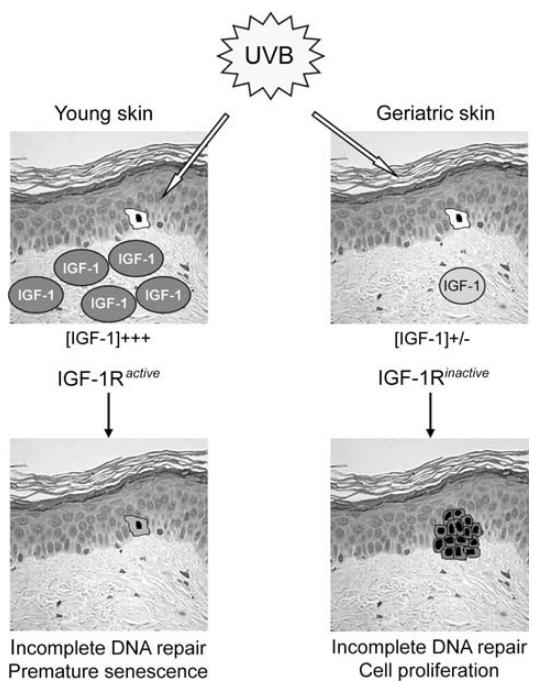
Der Einfluss des Alterns auf die Expression des insulinähnlichen Wachstumsfaktors 1 (IGF-1) in der Haut und seine Rolle bei der durch UVB-induzierten Karzinogenese.
Studien haben gezeigt, dass IGF-1 auch die Haut vor den Auswirkungen des Alterns schützen kann. Durch die Förderung der Kollagensynthese und die Reduzierung des Abbaus von Kollagenfasern hilft IGF-1, die Elastizität und Festigkeit der Haut zu erhalten. Dieser Anti-Aging-Effekt ist besonders wichtig, um die Bildung von Falten zu verhindern und einen glatten, jugendlichen Teint zu bewahren. Darüber hinaus wurde festgestellt, dass IGF-1 Entzündungen in der Haut reduziert, was dazu beitragen kann, chronische Hauterkrankungen zu verhindern und die allgemeine Hautgesundheit zu verbessern (Muraguchi et al., 2019).
Auswirkungen auf Nervengewebe
IGF-1 hat signifikante neuroprotektive Wirkungen und verbessert das Überleben und die Funktion von Neuronen. Es erhöht den Glukosetransport in die Neuronen und versorgt sie mit der Energie, die sie für ihre ordnungsgemäße Funktion benötigen. Dies ist besonders wichtig bei niedrigen Glukosespiegeln, bei denen IGF-1 hilft, neuronale Schäden und den Zelltod zu verhindern. Darüber hinaus stimuliert IGF-1 die Synthese von neuronaler RNA und fördert die Bildung von Axonen, den langen Fortsätzen der Neuronen, die Nervensignale übertragen (Dyer et al., 2016).
Im Nervensystem fördert IGF-1 auch die Proliferation von Gliazellen, die Neuronen unterstützen und schützen. Zu diesen Gliazellen gehören Astrozyten, Oligodendrozyten und Mikroglia, die jeweils eine entscheidende Rolle bei der Erhaltung der Gesundheit und Funktion des Nervensystems spielen. Durch die Förderung der Proliferation und Funktion dieser Zellen hilft IGF-1, ein unterstützendes Umfeld für Neuronen zu schaffen, das ihr Wachstum, ihre Reparatur und ihr Überleben erleichtert (Carson et al., 1993).
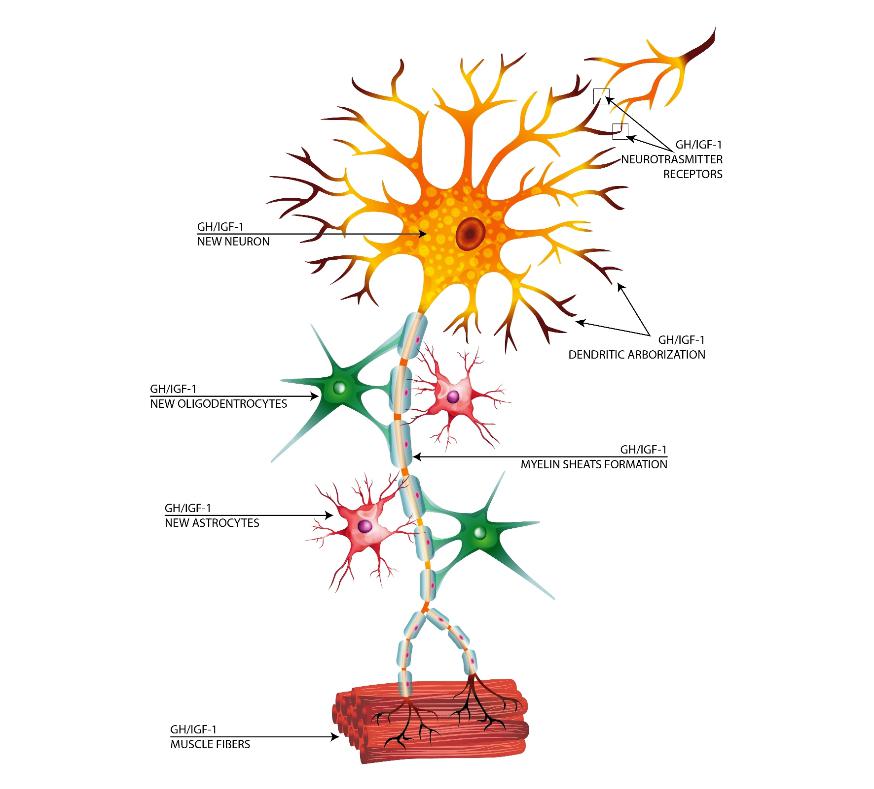
Die neuroprotektiven Effekte von IGF-1 sind besonders relevant bei neurodegenerativen Erkrankungen wie Alzheimer und Parkinson. Untersuchungen haben gezeigt, dass IGF-1 die Ansammlung toxischer Proteine, wie Beta-Amyloid-Plaques bei Alzheimer, reduzieren und die Beseitigung dieser Proteine aus dem Gehirn fördern kann. Dies schützt Neuronen vor Schäden und unterstützt die kognitive Funktion. Darüber hinaus wurde festgestellt, dass IGF-1 die Regeneration beschädigter Neuronen fördert, was potenzielle therapeutische Vorteile für neurodegenerative Erkrankungen bietet (Dyer et al., 2016).
Auswirkungen auf das Herz-Kreislauf-System
IGF-1 spielt eine spezialisierte Rolle für die Herz-Kreislauf-Gesundheit, indem es die Entwicklung und Funktion des Herzens und der Blutgefäße fördert. Es verbessert das Herzzeitvolumen, das Schlagvolumen, die Kontraktilität und die Auswurffraktion, die alle für die Aufrechterhaltung einer effizienten Herzfunktion entscheidend sind. IGF-1 stimuliert auch die Umstrukturierung von Herzgewebe, hilft bei der Reparatur von Schäden nach einem Myokardinfarkt und verbessert die allgemeine Herzgesundheit (Macvanin et al., 2023).
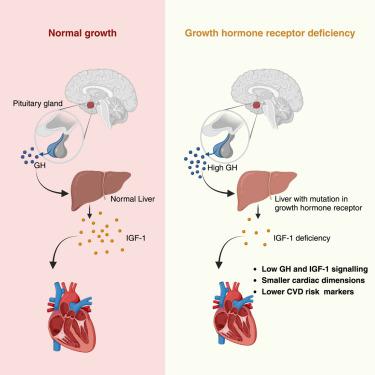
Die kardiovaskulären Wirkungen von IGF-1 werden durch mehrere Mechanismen vermittelt. Erstens fördert IGF-1 die Proliferation und das Überleben von Kardiomyozyten, den Muskelzellen des Herzens. Dies hilft, die strukturelle Integrität und die Kontraktilitätsfunktion des Herzens aufrechtzuerhalten. Zweitens stimuliert IGF-1 die Angiogenese, die Bildung neuer Blutgefäße, was die Durchblutung und Sauerstoffversorgung des Herzens und anderer Gewebe verbessert. Drittens hat IGF-1 anti-apoptotische und entzündungshemmende Wirkungen, die den Zelltod und die Entzündungen im Herz-Kreislauf-System reduzieren (De Giorgi et al., 2022).
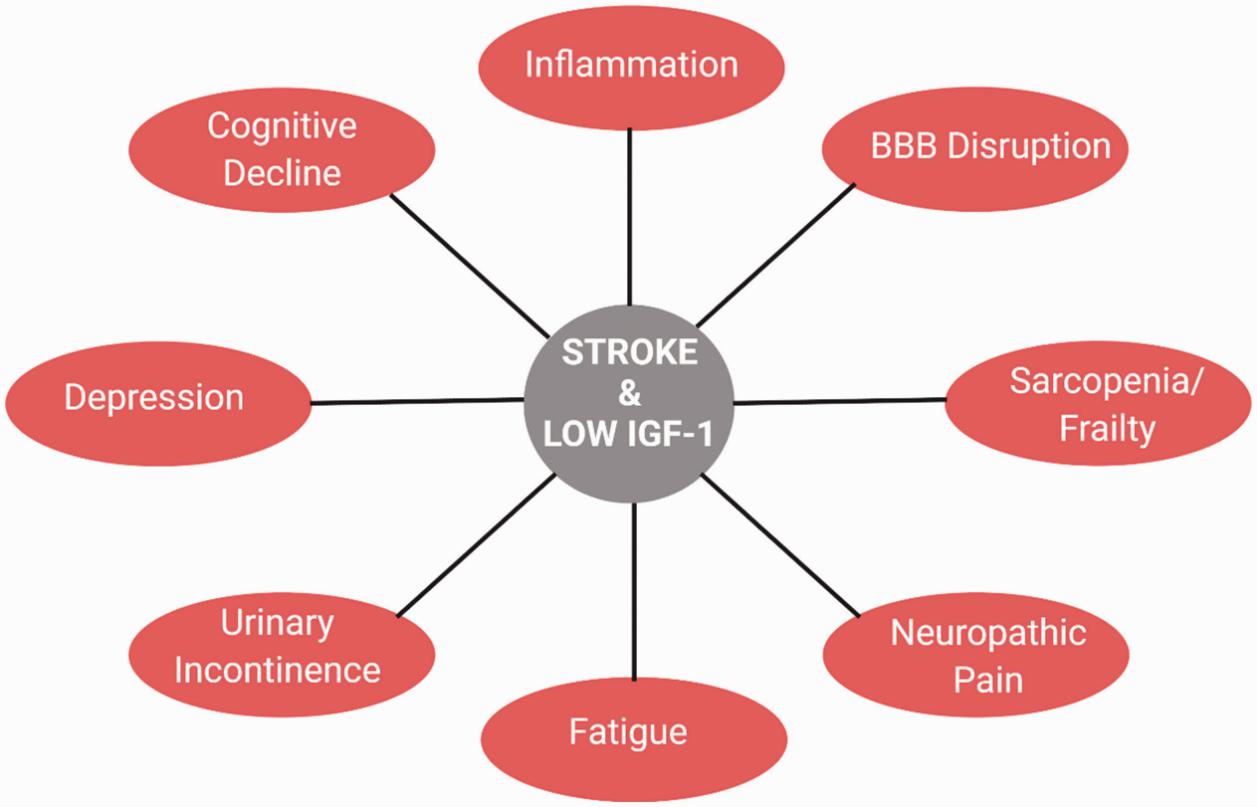
Klinische Studien haben gezeigt, dass niedrige IGF-1-Spiegel mit einem erhöhten Risiko für Herz-Kreislauf-Erkrankungen, einschließlich koronaren Herzkrankheiten und Schlaganfällen, verbunden sind. Umgekehrt werden höhere IGF-1-Spiegel mit einer besseren Herz-Kreislauf-Gesundheit und einem reduzierten Risiko für diese Erkrankungen in Verbindung gebracht. Beispielsweise zeigte eine prospektive Kohortenstudie, dass Teilnehmer mit höheren IGF-1-Spiegeln ein um 55% geringeres relatives Risiko für einen Myokardinfarkt hatten als diejenigen mit niedrigeren Spiegeln (Macvanin et al., 2023).
Auswirkungen auf die Immunität
IGF-1 hat einen erheblichen Einfluss auf das Immunsystem, da es die Funktion und Proliferation verschiedener Immunzellen verbessert. Es erhöht die Populationen von T-Lymphozyten, B-Lymphozyten und natürlichen Killerzellen, die alle eine entscheidende Rolle bei der Abwehr des Körpers gegen Infektionen und Krankheiten spielen. IGF-1 steigert auch die Aktivität der T-Lymphozyten, die für die zellvermittelte Immunität und die Zerstörung infizierter oder krebserkrankter Zellen unerlässlich sind (Alpdogan et al., 2003).
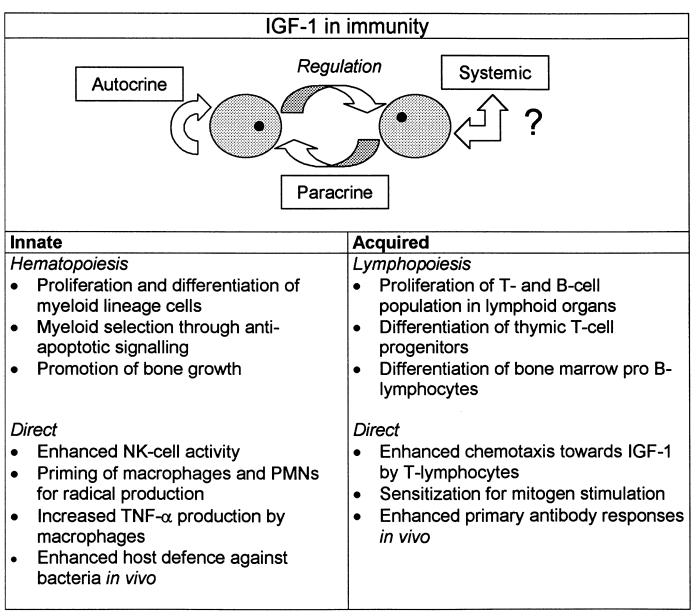
Die immunsystemstärkenden Effekte von IGF-1 werden durch mehrere Mechanismen vermittelt. IGF-1 stimuliert die Proliferation von Immunzellen, indem es an seine Rezeptoren auf deren Oberfläche bindet, was zu einer erhöhten Zellteilung und -wachstum führt. Dies ist besonders wichtig für die Erweiterung der Immunzellpopulationen als Reaktion auf Infektionen oder immunologische Herausforderungen. Darüber hinaus verbessert IGF-1 die Funktion dieser Zellen, indem es ihre Aktivierung fördert und ihre Fähigkeit erhöht, auf Krankheitserreger zu reagieren (Dyer et al., 2016).
Forschungen haben gezeigt, dass IGF-1 auch Immunzellen vor Apoptose, also dem programmierten Zelltod, schützen kann, was entscheidend für die Aufrechterhaltung einer robusten Immunantwort ist. Beispielsweise haben Studien gezeigt, dass IGF-1 die Apoptose von Makrophagen und Neutrophilen hemmen kann, zwei wesentliche Arten von Immunzellen, die an der initialen Reaktion des Körpers auf Infektionen beteiligt sind. Durch die Erhaltung der Lebensfähigkeit dieser Zellen trägt IGF-1 dazu bei, eine effektive und nachhaltige Immunantwort zu gewährleisten (Alpdogan et al., 2003).
Anwendung von IGF-1 LR3
IGF-1 LR3 ist oft das geheime Mittel von professionellen Bodybuildern. Die Verwendung dieses Produkts ist der nächste Schritt für Fortschritte nach anabolen Steroiden und Wachstumshormonen, die seit langem in der Welt der PED-Liebhaber populär sind.
Das IGF-1 LR3-Produkt hat eine sehr breite Wirkung und kann sowohl zum Fettabbau, zur Beschleunigung der Heilung von Verletzungen und zur Stärkung des Gelenk-Band-Apparats, zum Muskelaufbau und zur beschleunigten Erholung nach Anstrengung eingesetzt werden, da die Substanz auch die Erholung des Nervensystems beeinflusst. IGF-1 LR3 bietet eine breite Palette von Eigenschaften, die für viele Zwecke geeignet sind und eine ausgezeichnete Ergänzung für jeden Ihrer Kuren darstellen, sei es für Muskelaufbau oder für das vorwettkampfmäßige Training.
Dosis:
Anfänger: 20-40 mcg pro Tag
Fortgeschrittene: 40-60 mcg pro Tag
Erfahrene: 60-100 mcg pro Tag
Zyklusdauer:
Typischerweise 4-6 Wochen, gefolgt von einer Pause gleicher Länge, um eine Desensibilisierung zu vermeiden.
Verabreichungsplan:
Häufigkeit: Tägliche Injektionen
Zeitpunkt: Morgens oder nach dem Training verabreichen, um die Absorption und Wirksamkeit zu maximieren.
Injektionsstelle: Subkutane oder intramuskuläre Injektionen, Stellen wechseln, um Gewebeschäden zu vermeiden.
Beispiel
| Zeitraum (Wochen) | Tägliche IGF-1 LR3-Dosis |
|---|---|
| 1-6 | 20-100 mcg (Erwägen, mit niedrigerer Dosis zu beginnen, um die Verträglichkeit zu überprüfen) |
| 7-12 | Auswaschphase |
| 13-18 | 20-100 mcg |
| 19-24 | Auswaschphase |
Überdosierung
Eine Überdosierung kann die oben aufgeführten Nebenwirkungen verursachen. Am häufigsten ist dies Hypoglykämie – eine Verringerung des Zuckers unter die 3,5 mmol/l-Marke. In diesem Fall ist es notwendig, eine bestimmte Menge Kohlenhydratnahrung zu sich zu nehmen, bis sich der Zustand stabilisiert.
Verabreichungsmethode
Intramuskuläre oder subkutane Injektionen mit Insulinspritzen.
Nachweis bei Dopingtests
Wenn Sie die Einnahme des Medikaments drei Tage vor dem Test stoppen, wird die Substanz im Blut nicht nachweisbar sein.
Potenzielle Risiken
Unter den Fans von PEDs gibt es Informationen, die IGF-1 mit der Entwicklung von Krebs in Verbindung bringen. Obwohl diese angebliche Korrelation großen Einfluss auf die Massenmedien hat, haben bisher die meisten klinischen und epidemiologischen Berichte keine kausale Beziehung zwischen Wachstumshormontherapie und folglich einem Anstieg der IGF-1-Spiegel sowie einem erhöhten Krebsrisiko gezeigt (Werner & Laron., 2020).
Basierend auf diesen Daten verursacht das IGF-1-Medikament selbst keine Onkologie, sondern hat nur eine Kontraindikation zur Anwendung, wenn bereits Krebs oder eine Prädisposition dafür (hohe Krebsmarker) vorliegt. Wachstumshormon und IGF-1 sind, selbst in hohen pharmakologischen Dosen, nicht in der Lage, eine maligne Transformation zu induzieren. Jedoch kann die GH-IGF1-Achse bereits transformierte Krebszellen durch verschiedene Phasen des Zellzyklus „vorantreiben“.
WIE MAN IGH-1 LR3 ANWENDET
Alle Peptidhormone in unserem Produktportfolio (außer Flüssigwachstumshormon) sind gefriergetrocknet. Peptide, die als gefriergetrocknetes Pulver geliefert werden, kommen mit einem Lösungsmittel (bakteriostatisches Wasser in einer 1-ml-Ampulle). Dieses Lösungsmittel wird zur Herstellung einer Lösung verwendet, die dann in flüssiger Form aufbewahrt wird.
Ampulle mit Lösungsmittel (bakteriostatisches Wasser)
In einer wässrigen Umgebung zersetzen sich Peptide schnell. Dies liegt zum Teil an der Anwesenheit von Bakterien, für die Wasser ein ideales Umfeld für Wachstum und Fortpflanzung bietet. Das Injektionswasser ist steril. Sobald jedoch die Verpackung (normalerweise eine Ampulle oder Fläschchen) geöffnet wird, ist die Sterilität beeinträchtigt. Um die Sterilität so lange wie möglich aufrechtzuerhalten, wird Benzylalkohol oder Metakresol wegen seiner starken antibakteriellen Eigenschaften hinzugefügt. Dieses behandelte Wasser wird als bakterienstatisch bezeichnet, was bedeutet, dass Bakterien in einem „statischen Zustand“ bleiben und sich nicht vermehren. Wachstumshormon und andere Peptide können in einem bakterienstatischen Umfeld ihre Stabilität aufrechterhalten und der Zersetzung viel länger widerstehen.
Wie man die Lösung vorbereitet
- Füllen Sie die Spritze mit Wasser. In der Regel werden die Flascheninhalte in einem Milliliter Wasser aufgelöst.
- Fügen Sie Wasser zur Flasche mit dem gefriergetrockneten Pulver hinzu. Neigen Sie die Flasche so, dass die Nadel die Wand der Flasche berührt.
- Vermeiden Sie es, dass das Verdünnungsmittel direkt mit dem gefriergetrockneten Pulver in Kontakt kommt. Das Verdünnungsmittel sollte langsam an den Seiten der Flasche herunterfließen (nicht auf einmal eingießen und Eile vermeiden).
- Nachdem das gesamte Lösungsmittel zur Flasche mit dem Peptid hinzugefügt wurde, schwenken Sie die Flasche vorsichtig (aber nicht schütteln), bis sich das gefriergetrocknete Pulver aufgelöst hat und Sie eine klare Flüssigkeit erhalten. Die Lösung ist nun einsatzbereit.
- Bewahren Sie die vorbereitete Lösung bei einer Temperatur von 2-8°C auf.
Sehen Sie sich das Video zur Zubereitung der Lösung an ⤵️
https://t.me/driadaeducation/52
Spritzen für Injektionen
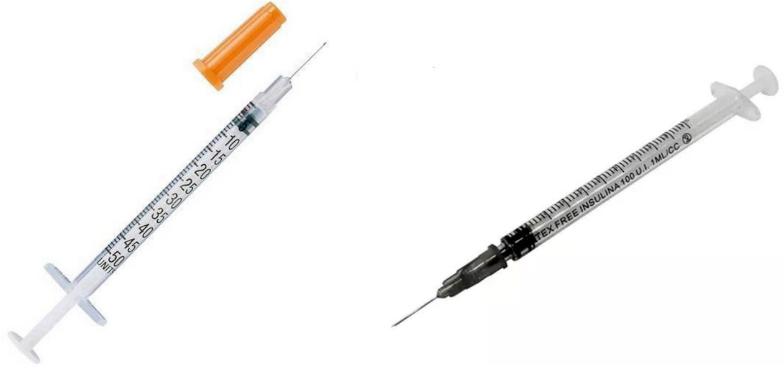
Es wird empfohlen, Spritzen zu verwenden, die frisch aus der Verpackung kommen, um eine Infektion zu vermeiden (die Wiederverwendung von Spritzen erhöht das Infektionsrisiko). Insulinspritzen werden normalerweise für subkutane Injektionen verwendet und können entweder eine abnehmbare Nadel oder eine feste Nadel haben. Eine der beliebtesten Injektionsnadeln ist die G30. Spritzen sind normalerweise in Größen von 1 ml und 0,5 ml erhältlich.
Insulinspritzen gibt es in den Formaten U40 und U100, die dem Insulininhalt von 40 Einheiten pro 1 ml bzw. 100 Einheiten pro 1 ml entsprechen. Jede Spritze ist speziell für eine bestimmte Insulinart ausgelegt. Dies gilt jedoch nicht für Einheiten von Wachstumshormon oder mg von Peptiden, sodass beide Spritzentypen mit entsprechenden Anpassungen verwendet werden können, um die richtige Dosierung zu bestimmen. Diese Spritzen haben unterschiedliche Markierungen, und anhand dieser Markierungen können Sie die Anzahl der Einheiten von Wachstumshormon bestimmen, die injiziert werden sollen. Im Folgenden zeigen wir ein Bild, das die Dosierung verschiedener Peptide bei Mischung mit 1 ml Wasser für U100- und U40-Spritzen zeigt.

Subkutane Injektionen
Nachdem das Peptid mit Wasser verdünnt wurde, ist es einsatzbereit. Alle Peptide werden subkutan oder intramuskulär mit einer Insulinspritze injiziert.
Sie benötigen:
- Alkoholpad
- Insulinspritze
- Flasche mit der vorbereiteten Lösung
Injektionsverfahren:
- Entfernen Sie die Flaschenabdeckung.
- Wischen Sie den Gummistopfen der Flasche mit Alkohol ab.
- Nehmen Sie eine Insulinspritze und stecken Sie sie in die Flasche.
- Ziehen Sie die benötigte Menge Lösung in die Spritze auf.
- Wischen Sie die Injektionsstelle mit einem Alkoholpad ab.
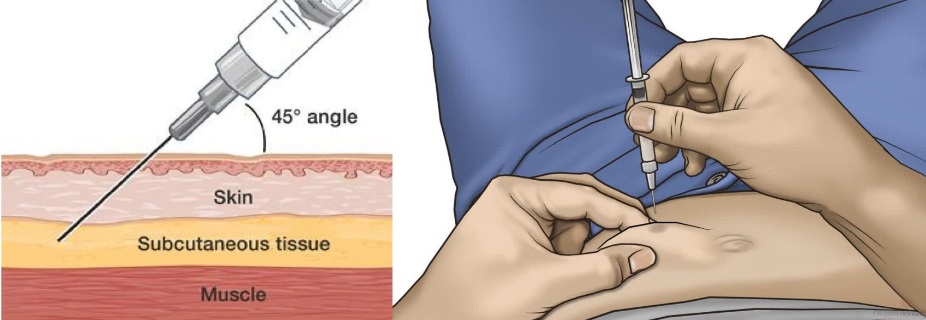
- Halten Sie die Nadel in einem Winkel von 30-45 Grad und injizieren Sie.
- Injizieren Sie die Lösung langsam.
- Halten Sie die Nadel nach dem Abschluss für 10 Sekunden in der Position, bevor Sie sie entfernen, um ein Auslaufen der injizierten Flüssigkeit zu verhindern.
- Synergistischer Zuwachs an Muskelmasse
- Synergistischer Effekt der Fettverbrennung
- Verstärkung der Wirkung anaboler Steroide
- Synergistischer Effekt auf die Stärkung des Knochengewebes
- Synergistischer Zuwachs an Muskelmasse
- Synergistischer Effekt der Fettverbrennung
- Synergistischer Effekt auf die Sehnenreparatur
- Synergistischer Effekt auf die Stärkung des Knochengewebes
- Erhöhtes Risiko von Nebenwirkungen durch übermäßige IGF-1-Spiegel
- Synergistischer Zuwachs an Muskelmasse
- Erhöhtes Risiko für Hypoglykämie
Lagerung
Die richtige Lagerung von Peptid-Arzneimitteln ist entscheidend für die Aufrechterhaltung ihrer Wirksamkeit. Im Folgenden finden Sie die Richtlinien zur Lagerung von Peptiden in verschiedenen Formen.
Lagerung der Pulverform
Die Pulverform (ungemischt) kann bei Raumtemperatur oder im Kühlschrank aufbewahrt werden. Das lyophilisierte Pulver sollte vor direkter Sonneneinstrahlung und übermäßiger Hitze geschützt werden. Unter geeigneten Lagerbedingungen können Peptide in trockener Form bis zu 3 Jahre bei 2-8°C und bis zu 2 Jahre bei 15-30°C aufbewahrt werden. Wenn die Ampulle beschädigt ist und Luft eindringt, wird der Wirkstoff außerhalb des Kühlschranks schnell abgebaut und behält innerhalb von zwei Wochen nur noch etwa die Hälfte seiner Konzentration. Daher ist es am besten, das Peptid im Kühlschrank zu lagern, wenn die Unversehrtheit der Verpackung unsicher ist.
Lagerung des bakteriostatischen Wassers
Bakteriostatisches Wasser sollte immer im Kühlschrank bei 2-8°C aufbewahrt werden, um seine Eigenschaften zu erhalten. Wenn das Peptid und das bakteriostatische Wasser zusammen gelagert werden, sollte das gesamte Set im Kühlschrank aufbewahrt werden.
Lagerung der Lösung
Nach dem Mischen des Pulvers mit Wasser aus der Ampulle muss die Peptidlösung im Kühlschrank aufbewahrt werden. Ohne Kühlung beginnt das Peptid sich zu zersetzen, und innerhalb weniger Tage werden die Moleküle vollständig abgebaut. Die Lagerdauer für jedes Peptid variiert. Zum Beispiel kann Wachstumshormon nur 2-3 Tage im Kühlschrank aufbewahrt werden, während HCG etwa 5 Wochen haltbar ist. Im Durchschnitt können andere Peptide mindestens 30 Tage aufbewahrt werden, wobei einige sogar noch länger haltbar sein können. Die Abbaurate hängt auch von der Anzahl der Bakterien ab, die beim Durchstechen der Ampulle eingeführt werden, was bis zu einem gewissen Grad unvermeidlich ist.
!!! NIE PEPTIDE IM GEFRIERSCHRANK LAGERN !!!
Verwendung mit anabolen Steroiden
Es ist auch völlig angemessen, IGF-1 zusammen mit anabolen Steroiden und anderen Medikamenten mit ähnlichen Effekten zu verwenden. IGF-1 verstärkt die Effekte von anabolen Steroiden, indem es die Anzahl der Androgenrezeptoren erhöht. Das Medikament IGF-1 ist ein extrem starkes Anabolikum, das in Kombination mit AS einen sehr großen Zuwachs an fettfreier Muskelmasse bewirkt. Gleichzeitig hat IGF-1 viele andere nützliche Eigenschaften, die zusammen das maximale Umfeld für Wachstum schaffen.
Alle anabolen Steroide wirken auf die Muskeln durch spezielle Strukturen – Rezeptoren. Es gibt die Meinung, dass bei längerer Anwendung von Steroiden die Anzahl dieser Rezeptoren abnimmt. Auch die Anzahl dieser Rezeptoren nimmt mit dem Alter ab. In diesem Fall wird es notwendig, große Dosen von Steroiden zu verwenden. Mit 20 Jahren wirkt 300 mg Testosteronpropionat stärker als mit 30 Jahren. Mit 30 Jahren werden 600 mg für denselben Effekt benötigt. IGF-1 aktiviert Zellen und erhöht die Anzahl der Androgenrezeptoren, und mit 30 Jahren wirkt 300 mg Testosteronpropionat dann genauso wie mit 20 Jahren.
Effekte
Verwendung mit Wachstumshormon (Somatropin)
Die gleichzeitige Verwendung von Somatotropin kann ratsam sein, obwohl es auf den ersten Blick nicht logisch erscheinen mag, tun es jedoch viele professionelle Bodybuilder genau so. Bei gleichzeitiger Anwendung summieren sich ihre Effekte – als anabolischer Effekt für das Muskelwachstum und für die Wiederherstellung und Regeneration von Knorpel- und anderen Kollagenstrukturen. Auch Wachstumshormon und IGF-1 zusammen werden die Fettverbrennung erhöhen.
Es sollte bedacht werden, dass neben den positiven Effekten auch Nebenwirkungen auftreten können. Es sollte verstanden werden, dass der IGF-Spiegel bei der Verwendung beider Medikamente erheblich ansteigt, daher sollte eine solche Anwendung nicht über einen längeren Zeitraum erfolgen.
Effekte
Verwendung mit Insulin
Wie der Name IGF-1 andeutet, hat es eine Struktur, die Insulin ähnlich ist, und bindet nicht nur an seinen eigenen IGF1R-Rezeptor, sondern auch an den Insulinrezeptor – und umgekehrt. Die Bindungsaffinität für IGF1R und den Insulinrezeptor ist jedoch unterschiedlich, mit einer hohen Affinität von IGF-1 für IGF1R und etwa 10-mal geringerer Affinität für den Insulinrezeptor.
Auf der anderen Seite ist die Affinität von Insulin zu seinem eigenen Rezeptor etwa 100-mal höher im Vergleich zu IGF1R. Zudem zeigen IGF-1 und Insulin trotz der strukturellen Ähnlichkeit eine unterschiedliche Verteilung in Geweben, unterschiedliche Internalisierungs-Kinetiken und unterschiedliche subzelluläre Verteilung der hormonellen Rezeptoren. Folglich können beide Hormone ähnliche Wege beeinflussen, jedoch in unterschiedlichem Maße und zudem unterschiedliche andere Wege, die weiter unten liegen, unterschiedlich aktivieren.
Diese Hormone können im Hinblick auf ihre Wirkung auf den Glukosestoffwechsel im Körper verglichen werden. Bei gleichzeitiger Anwendung wird eine solche Nebenwirkung wie Hypoglykämie (ein Abfall des Zuckergehalts) so ausgeprägt sein, dass sie Lebensgefahren darstellen kann.