- Disponibilité: En stock
- Package: 1mg/vial+water
Poser une question sur ce produit
Le Long Arginine 3-IGF-1, abrégé en IGF-1 LR3 ou LR3-IGF-1, est une protéine synthétique et un analogue allongé du facteur de croissance de type insulinique humain 1 (IGF-1).
QU'EST-CE QUE L'IGF-1 ?
Le facteur de croissance de type insulinique 1 (IGF-1) est une protéine vitale qui joue un rôle essentiel dans la croissance et le développement humain. Cette protéine humaine recombinante, qui appartient à la famille des facteurs de croissance de type insulinique, se compose de 70 acides aminés et fonctionne de manière similaire à l'insuline. Elle est impliquée dans la régulation de divers processus corporels, notamment la croissance, le développement et la différenciation cellulaire, par le biais des voies endocrines, autocrines et paracrines.
L'un des aspects intrigants de l'IGF-1 est sa connexion avec le vieillissement. Des recherches suggèrent que des mutations dans le gène IGF-1 peuvent augmenter la durée de vie des animaux de laboratoire, soulignant son impact potentiel sur la longévité. Chez les enfants, l'IGF-1 est essentiel pour stimuler la croissance et la différenciation cellulaire, tandis que chez les adultes, il continue d'exercer des effets anabolisants, favorisant la croissance et le maintien des tissus.
L'IGF-1 fonctionne dans un réseau complexe de facteurs de croissance, de récepteurs et de protéines de liaison qui modulent la prolifération cellulaire, la différenciation et l'apoptose. Ces facteurs de croissance sont des protéines de faible poids moléculaire présentes dans presque tous les tissus, où elles régulent la division, la croissance et la migration cellulaire. Dans la peau, par exemple, ils sont essentiels à la migration et au développement des cellules épithéliales et stimulent la division cellulaire.
Souvent appelé somatomédine C, l'IGF-1 sert de médiateur clé des effets de l'hormone de croissance (HGH). Il est principalement produit par les hépatocytes du foie en réponse à la stimulation par l'hormone de croissance. La production d'IGF-1 par le foie est influencée par diverses hormones, notamment les stéroïdes sexuels, les hormones thyroïdiennes, les glucocorticoïdes et l'insuline. L'insuline, les androgènes et les œstrogènes ont tendance à augmenter la sécrétion d'IGF-1, tandis que les glucocorticoïdes l'inhibent. Cette interaction explique la synergie entre ces hormones dans les processus de croissance et de développement, ainsi que l'impact inhibiteur des glucocorticoïdes sur la croissance et la puberté.
Tout au long de la vie, les niveaux d'IGF-1 fluctuent, atteignant un pic pendant l'adolescence et diminuant pendant l'enfance et la vieillesse. Malgré ces variations, l'IGF-1 reste une hormone anabolique cruciale. Il est sécrété par divers tissus, le foie étant la principale source, libérant l'IGF-1 dans le sang pour agir comme une hormone endocrine. D'autres tissus, notamment les cellules cartilagineuses, sécrètent également l'IGF-1, où il fonctionne localement comme une hormone paracrine.
Ces dernières années, l'IGF-1 a attiré l'attention dans le monde du sport en tant qu'agent dopant, apparaissant dans de nombreux cas de dopage de haut niveau. Sa capacité à améliorer la croissance et les performances en fait une substance d'intérêt et de préoccupation dans les communautés sportives.
QUELLE EST LA DIFFÉRENCE ENTRE L'IGF-1 ET L'IGF-1 LR3 ?
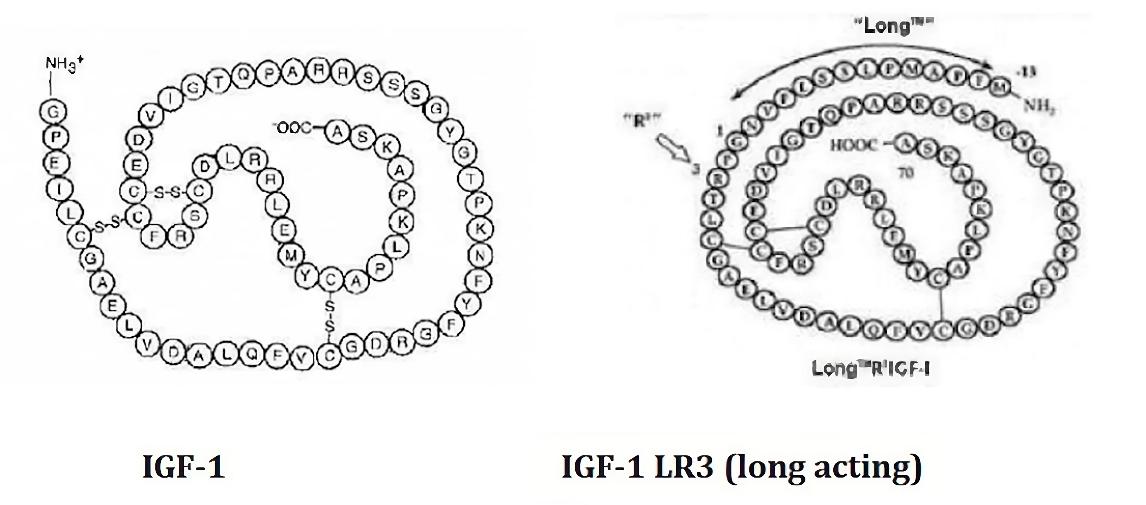
Le facteur de croissance de type insulinique 1 (IGF-1) et sa variante prolongée, IGF-1 LR3, partagent de nombreuses similitudes mais présentent également des différences distinctes qui influencent leurs fonctions et applications. L'IGF-1 est une protéine naturellement présente dans le corps humain, essentielle à la croissance, au développement et à la différenciation cellulaire. Il se compose de 70 acides aminés et agit en se liant aux récepteurs IGF-1, influençant divers processus physiologiques.
L'IGF-1 LR3, quant à lui, est une forme modifiée de l'IGF-1, conçue pour avoir une demi-vie plus longue et une stabilité accrue. Cette variante comprend 13 acides aminés supplémentaires à l'extrémité N-terminale, remplaçant l'acide glutamique original par une arginine au troisième acide aminé. Cette modification réduit considérablement l'affinité de liaison de l'IGF-1 LR3 aux protéines de liaison IGF, qui régulent généralement la disponibilité et l'activité de l'IGF-1. En conséquence, l'IGF-1 LR3 reste actif plus longtemps dans le sang, augmentant son efficacité dans la promotion de la croissance et des processus anabolisants.
La demi-vie prolongée de l'IGF-1 LR3 le rend particulièrement précieux dans les contextes médicaux et sportifs. Dans les contextes médicaux, il offre des avantages thérapeutiques potentiels pour les conditions nécessitant une activité prolongée de l'IGF-1, telles que les maladies de perte musculaire et les carences en croissance. Dans les sports et le culturisme, son action prolongée et ses effets anabolisants puissants en font un agent recherché pour améliorer la croissance musculaire et les performances. Cependant, cela soulève également des préoccupations quant à son utilisation abusive et aux implications éthiques dans les sports de compétition.
En résumé, bien que l'IGF-1 et l'IGF-1 LR3 jouent des rôles vitaux dans la croissance et le développement, la principale différence réside dans la structure modifiée de l'IGF-1 LR3, qui confère une demi-vie plus longue et une plus grande puissance. Cette distinction élargit non seulement ses applications thérapeutiques potentielles, mais souligne également la nécessité d'une régulation stricte pour prévenir les abus dans les environnements sportifs.
PRINCIPAUX EFFETS
L'IGF-1 est un anabolisant extrêmement puissant, qui, en combinaison avec des stéroïdes anabolisants, permet une très grande augmentation de la masse musculaire maigre. En même temps, l'IGF-1 possède de nombreuses autres propriétés utiles qui, ensemble, créent un effet de croissance maximal. L'IGF-1 est un produit qui peut augmenter vos résultats lorsque d'autres méthodes n'ont plus d'effet significatif.
Effets anabolisants
- Augmentation de la masse musculaire (divers modes d'exposition)
- Hyperplasie musculaire (propriété unique d'augmenter le nombre de cellules musculaires)
- Accélération de la synthèse des protéines
- Régénération des tissus tendineux (augmente la synthèse du collagène)
- A un effet réparateur sur les tissus cartilagineux
- Augmente l'efficacité des stéroïdes anabolisants (augmente le nombre de récepteurs aux androgènes)
- Restaure et renforce les tissus osseux et cartilagineux
Soutien du système cardiovasculaire
- Améliore le débit cardiaque, le volume systolique, la contractilité et la fraction d'éjection.
- Stimule la contractilité et le remodelage tissulaire chez l'homme pour améliorer la fonction cardiaque après un infarctus du myocarde.
- Améliore le profil lipidique
- Réduit les niveaux d'insuline, augmente la sensibilité à l'insuline et favorise le métabolisme du glucose
- Réduit le risque global de complications cardiovasculaires
- Aide à lutter contre les processus inflammatoires
Tissu nerveux
- Augmente le transport du glucose dans les tissus nerveux
- Protège les neurones en cas de faibles niveaux de glucose, empêchant la destruction des cellules.
- Joue un rôle important dans la restauration des neurones et des tissus nerveux en général
Autres effets
- Régule l'expression des gènes qui augmentent l'espérance de vie.
- Accélère la régénération de la peau, prévient le vieillissement cutané
- Amélioration de l'immunité
Mécanisme d'action
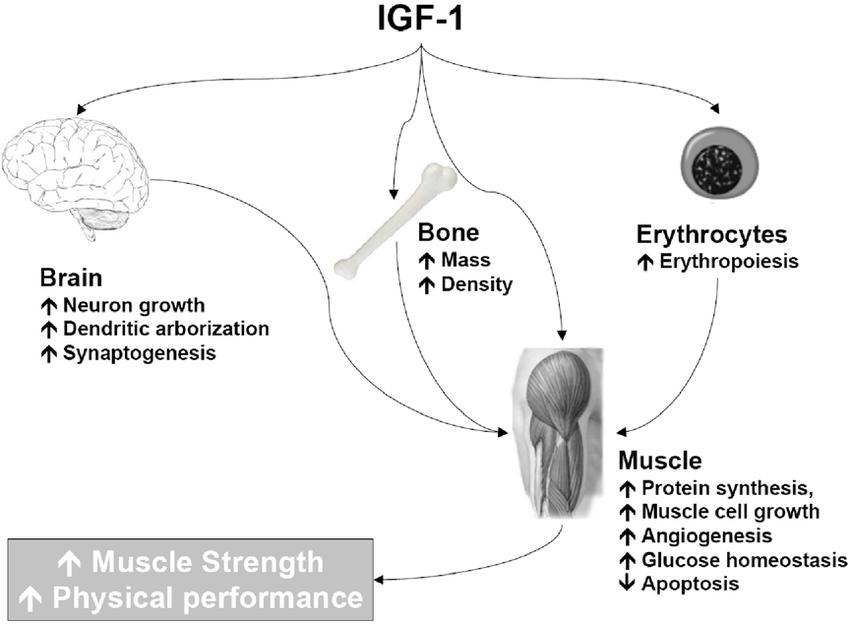
Le facteur de croissance similaire à l'insuline-1 (IGF-1) est une protéine vitale qui joue un rôle crucial dans la régénération et la réparation de divers tissus dans le corps humain, y compris les os, les muscles, la peau et le cartilage. Lorsque l'IGF-1 interagit avec les tissus osseux et cartilagineux, il se lie à des récepteurs spécifiques sur les ostéoblastes et les chondroblastes—les cellules responsables de la croissance et de la réparation des os et du cartilage. Cette liaison stimule l'activité métabolique de ces cellules, entraînant une guérison accélérée des fractures et autres blessures osseuses. L'IGF-1 réduit également l'inflammation dans les zones endommagées, améliorant l'activité des cellules impliquées dans le renouvellement des tissus (Yakar et al., 2019).
De plus, les effets métaboliques de l'IGF-1 vont au-delà de la croissance et de la réparation. Il joue un rôle important dans la signalisation des nutriments, coordonnant le métabolisme des protéines, des graisses et des glucides à travers différents types de cellules. Cela est réalisé grâce à la stimulation des récepteurs IGF-1, qui informent les cellules de la disponibilité des nutriments. Cette coordination aide à assurer que les cellules reçoivent les nutriments nécessaires à la croissance et à la maintenance. Comme l'insuline, l'IGF-1 est régulé par le statut nutritionnel et participe à l'homéostasie du glucose. Il abaisse les niveaux de glucose sanguin en augmentant l'absorption du glucose dans les cellules et en réduisant la sécrétion d'insuline, ce qui améliore la sensibilité à l'insuline (Samani et al., 2007).
En plus de son rôle dans le métabolisme, l'IGF-1 affecte également le métabolisme des protéines et la lipolyse. Il agit en synergie avec l'hormone de croissance (GH) pour améliorer la dégradation des graisses et promouvoir la cétogenèse. Cette synergie entre l'IGF-1 et la GH est cruciale pour maintenir l'équilibre énergétique et soutenir les processus de croissance. Des études ont montré que de faibles niveaux d'IGF-1 sont souvent associés au syndrome métabolique, un ensemble de conditions qui augmentent le risque de maladies cardiaques, d'accidents vasculaires cérébraux et de diabète. Cela met en évidence l'importance de l'IGF-1 dans le maintien de la santé métabolique globale (Clemmons, 2004).
Effets sur les muscles
L'IGF-1 a un impact profond sur les tissus musculaires, favorisant la croissance et la réparation des muscles. Cela est principalement réalisé grâce à la stimulation des cellules satellites, qui sont des cellules souches situées dans le tissu musculaire. Lorsque le tissu musculaire est endommagé, l'IGF-1 active ces cellules satellites, les faisant se multiplier et se différencier en nouvelles cellules musculaires. Ce processus répare non seulement les fibres musculaires endommagées mais entraîne également une augmentation de la masse musculaire. La capacité de l'IGF-1 à améliorer la régénération musculaire en fait un traitement clé pour les affections impliquant l'atrophie musculaire, telles que la dystrophie musculaire (Ahmad et al., 2020).
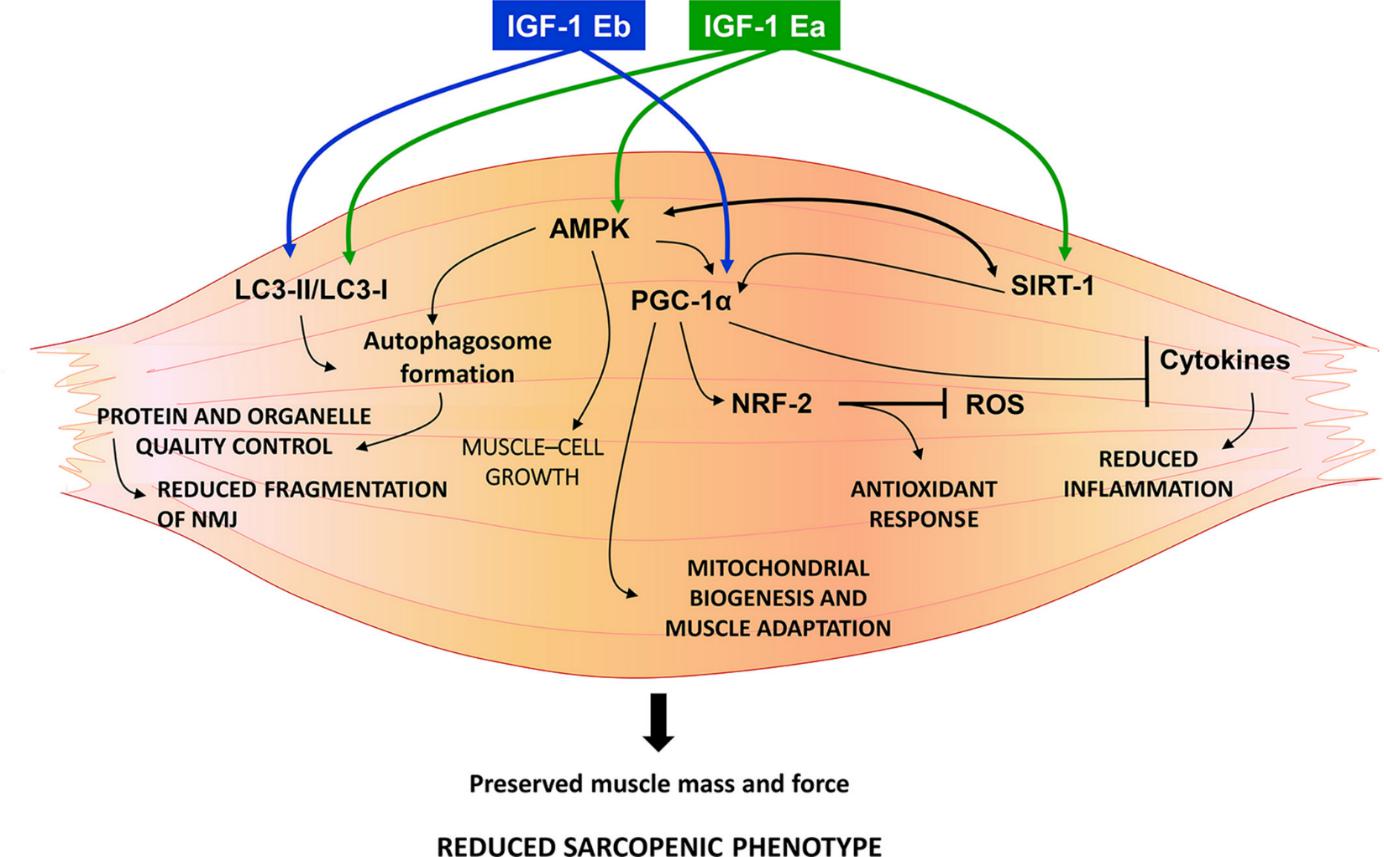
Les mécanismes moléculaires par lesquels l'IGF-1 stimule la croissance musculaire impliquent plusieurs voies de signalisation. L'une des principales voies est la voie PI-3 kinase, qui conduit à l'activation de la protéine kinase B (AKT). AKT favorise ensuite la synthèse des protéines en activant la voie mTOR, un régulateur crucial de la croissance cellulaire et de la synthèse des protéines. De plus, l'IGF-1 améliore le transport des acides aminés dans les cellules musculaires, fournissant les éléments constitutifs nécessaires à la synthèse des protéines. L'IGF-1 inhibe également la dégradation des protéines en réduisant l'expression des gènes impliqués dans l'atrophie musculaire, tels que MuRF1 et MAFbx (Lai et al., 2004).
En plus de ses effets anabolisants, l'IGF-1 possède également des propriétés anti-cataboliques. Il contrecarre les effets des cytokines inflammatoires qui favorisent la dégradation musculaire. En inhibant ces voies cataboliques, l'IGF-1 aide à préserver la masse et la fonction musculaires, même dans des conditions de stress ou de maladie. Ce double rôle de promotion de la croissance musculaire et de prévention de la dégradation musculaire fait de l'IGF-1 un facteur essentiel pour maintenir la santé et la fonction musculaires (Lai et al., 2004).
Effets sur le tissu tendineux
Les blessures aux tendons sont notoirement lentes à guérir, entraînant souvent des cicatrices fibrovasculaires qui altèrent les propriétés mécaniques des tendons et augmentent le risque de ré-injury. Il a été démontré que l'IGF-1 améliore considérablement la guérison des tendons en favorisant la prolifération cellulaire, la synthèse de l'ADN et la production de matrice, en particulier le collagène I, qui est le principal composant du tissu tendineux. Cela fait de l'IGF-1 un puissant agent anabolique pour améliorer la réparation et la fonction des tendons (Miescher et al., 2023).
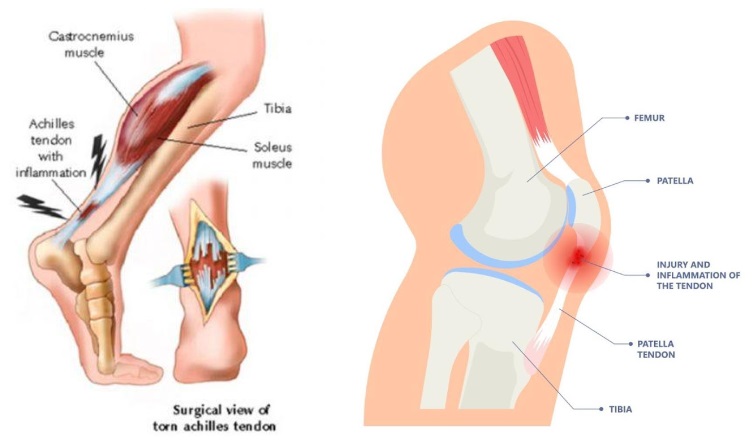
Le mécanisme par lequel l'IGF-1 favorise la guérison des tendons implique plusieurs processus cellulaires. Lorsqu'il est appliqué à des cultures de ténocytes—les cellules qui composent les tendons—l'IGF-1 stimule ces cellules à proliférer et à produire davantage de composants de la matrice extracellulaire, y compris le collagène. Cette production accrue de matrice fournit le soutien structurel nécessaire à la réparation des tendons. De plus, l'IGF-1 a montré qu'il réduisait l'inflammation dans le tendon blessé, ce qui soutient davantage le processus de guérison en créant un environnement plus favorable à la régénération des tissus (Disser et al., 2019).
Dans les modèles animaux précliniques et chez les patients humains, l'IGF-1 a démontré son efficacité pour améliorer les résultats de la guérison des tendons. Par exemple, des études ont montré que l'application d'IGF-1 aux tendons blessés dans des modèles animaux accélère le processus de guérison, réduit la formation de cicatrices et améliore les propriétés mécaniques des tendons guéris. Ces résultats suggèrent que l'IGF-1 pourrait être un agent thérapeutique précieux pour traiter les blessures tendineuses en milieu clinique. (Doessing et al., 2010)
Effets sur le tissu cartilagineux
L'IGF-1 joue un rôle crucial dans le maintien et la réparation du tissu cartilagineux, qui est essentiel pour la santé et la fonction des articulations. Le cartilage est un tissu élastique résilient et lisse qui recouvre et protège les extrémités des os longs au niveau des articulations. Il sert également de coussin entre les os, permettant des mouvements fluides et sans douleur. L'IGF-1 régule le métabolisme du cartilage en favorisant les processus anaboliques et en inhibant les processus cataboliques, maintenant ainsi l'intégrité et la fonction du cartilage (Wen et al., 2021).
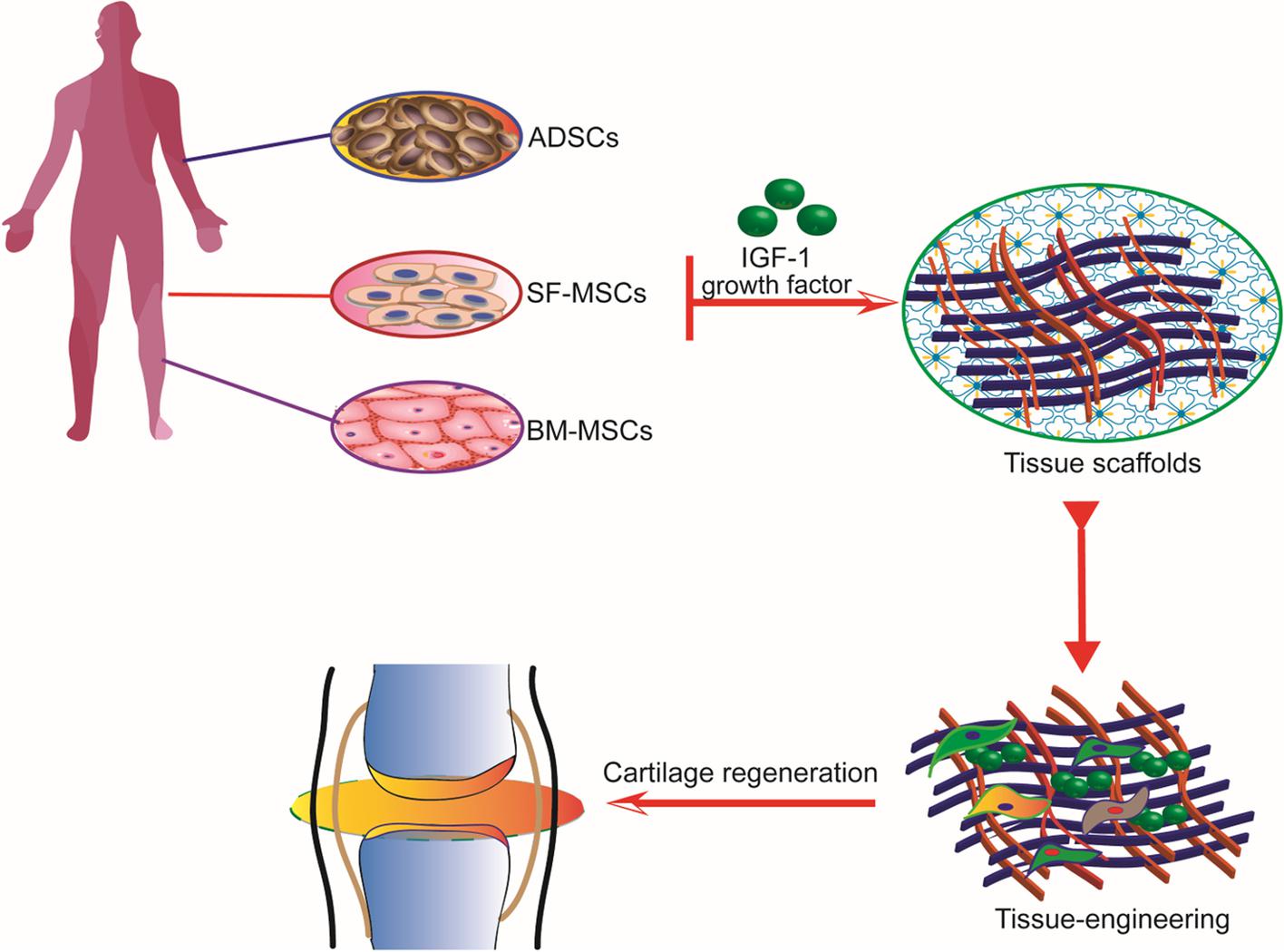
Les cellules principales responsables du maintien du cartilage sont les chondrocytes. L'IGF-1 stimule ces cellules à produire des composants de la matrice extracellulaire, tels que le collagène et les protéoglycanes, qui sont essentiels pour la structure et la fonction du cartilage. En plus de favoriser la synthèse de la matrice, l'IGF-1 inhibe l'activité des enzymes qui dégradent le cartilage, comme les métalloprotéinases matricielles (MMP). Cette double action de promotion des processus anaboliques et d'inhibition des processus cataboliques aide à préserver le tissu cartilagineux et à prévenir la dégénérescence (Vedadghavami, 2022).
Des études ont montré que l'IGF-1 peut ralentir la progression de l'arthrose, une maladie dégénérative des articulations caractérisée par la dégradation du cartilage. La délivrance efficace de l'IGF-1 au cartilage endommagé est cruciale pour ses effets thérapeutiques. Des techniques telles que les injections intra-articulaires et les systèmes de délivrance localisés sont explorées pour s'assurer que l'IGF-1 atteint le tissu cible en concentrations suffisantes. Des études animales ont démontré que l'administration continue d'IGF-1 peut prévenir la dégradation du cartilage et favoriser la réparation, soulignant son potentiel en tant que traitement de l'arthrose (Wen et al., 2021).
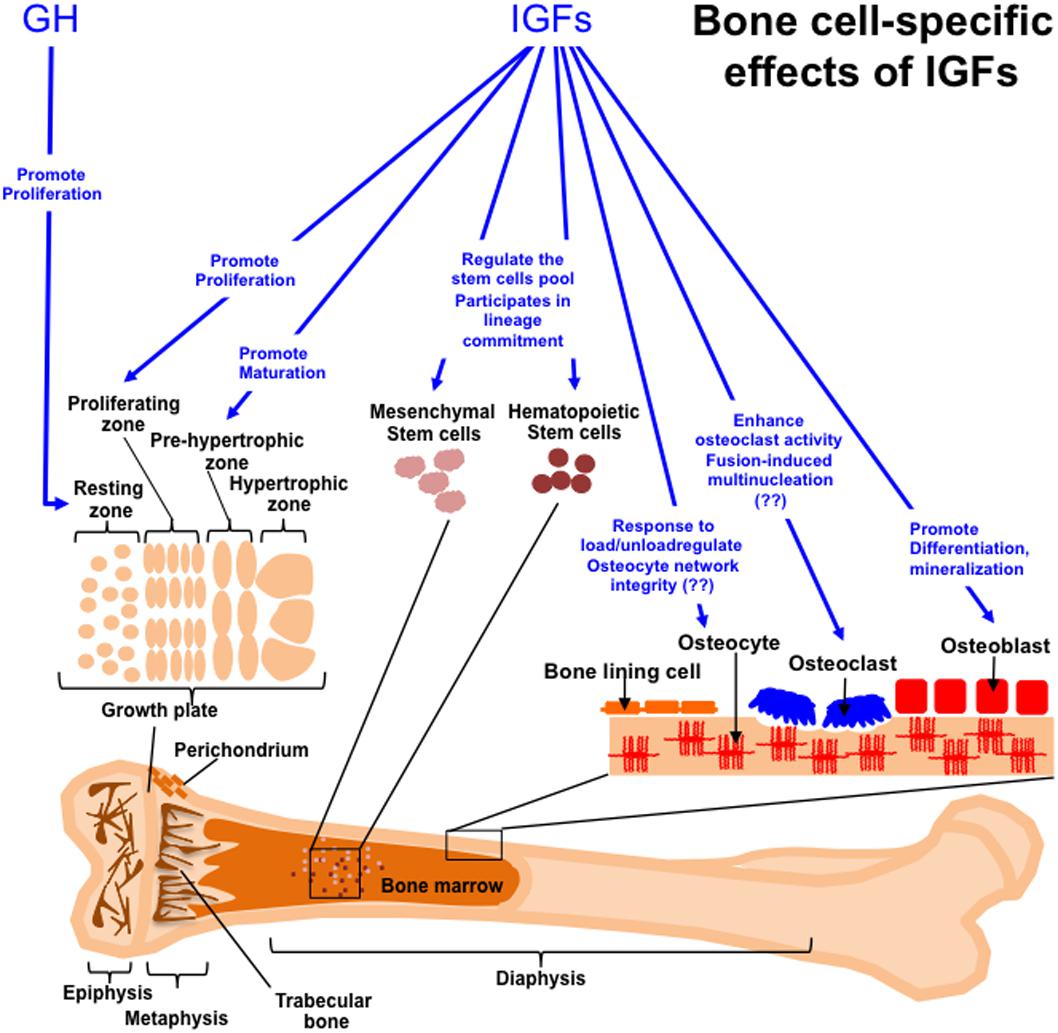
Tissu osseux
L'IGF-1 influence de manière significative le métabolisme osseux en favorisant à la fois la résorption et la formation osseuses. Cette double action est cruciale pour le remodelage osseux, un processus continu où le vieux tissu osseux est remplacé par du nouveau. L'IGF-1 stimule les ostéoblastes, les cellules responsables de la formation osseuse, à produire une nouvelle matrice osseuse. Il favorise également l'activité des ostéoclastes, les cellules responsables de la résorption osseuse, pour éliminer l'os ancien ou endommagé, facilitant ainsi le processus de remplacement (Canalis, 2009).
Les effets de l'IGF-1 sur la santé osseuse sont particulièrement évidents dans les conditions impliquant des fractures osseuses et l'ostéoporose. Des études ont montré que l'administration d'IGF-1 à des patients présentant des fractures peut accélérer la guérison osseuse et améliorer les résultats cliniques. Par exemple, il a été constaté que le traitement à l'IGF-1 augmente la densité minérale osseuse et améliore les propriétés structurelles de l'os guéri, le rendant plus fort et moins sujet à de nouvelles blessures (Locatelli & Bianchi., 2014).
En plus de ses effets directs sur les cellules osseuses, l'IGF-1 influence également la santé osseuse en interagissant avec d'autres hormones, telles que l'hormone parathyroïdienne (PTH) et la vitamine D. Ces interactions aident à réguler l'homéostasie du calcium et à garantir que les os reçoivent des nutriments adéquats pour la croissance et la réparation. En modulant ces voies hormonales, l'IGF-1 joue un rôle essentiel dans le maintien de la santé osseuse et la prévention de maladies telles que l'ostéoporose (Canalis, 2010).
IGF-1 et le métabolisme du glucose
L'IGF-1 a des effets significatifs sur le métabolisme du glucose, notamment en améliorant la sensibilité à l'insuline et en régulant les niveaux de glucose dans le sang. Il stimule le transport du glucose dans les cellules musculaires via les récepteurs IGF-1 ou les récepteurs hybrides insuline/IGF-1. En augmentant l'absorption de glucose dans les cellules musculaires, l'IGF-1 aide à abaisser les niveaux de glucose dans le sang, réduisant ainsi le besoin de sécrétion d'insuline (Clemmons, 2004).
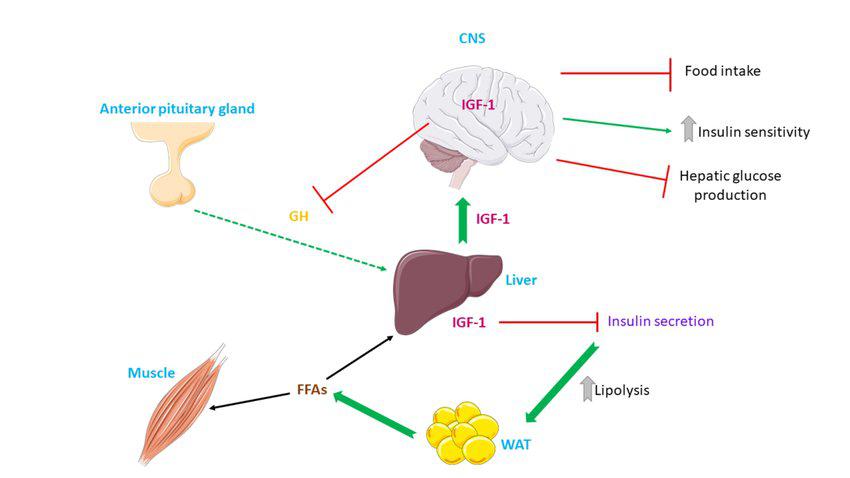
Description des actions métaboliques induites par l'IGF-1. L'IGF-1 est principalement libéré par le foie et améliore la sensibilité à l'insuline en supprimant la sécrétion d'insuline, ce qui entraîne une lipolyse accrue dans le tissu adipeux et favorise l'utilisation des NEFA dans les muscles et le foie. Abréviations utilisées : SNC : système nerveux central ; GH : hormone de croissance ; IGF-1 : facteur de croissance insulinique-1 ; AGNL : acides gras non liés ; TBA : tissu adipeux blanc.
Dans les modèles animaux, il a été démontré que des concentrations élevées d'IGF-1 libre inhibent la gluconéogenèse, le processus par lequel le glucose est produit à partir de sources non glucidiques dans le foie. Cette inhibition aide à réduire les niveaux de glucose dans le sang et améliore l'homéostasie globale du glucose. De plus, des études ont montré que la suppression du récepteur de l'insuline chez la souris réduit les niveaux de glucose sanguin en réponse à l'IGF-1, indiquant que l'IGF-1 peut en partie compenser le rôle de l'insuline dans le métabolisme du glucose (Clemmons, 2004).
Des études cliniques ont également mis en évidence l'importance de l'IGF-1 dans le maintien du métabolisme du glucose. Par exemple, des recherches ont montré que de faibles niveaux de sérum IGF-1 sont associés à une tolérance au glucose altérée et à un risque accru de diabète de type 2. À l'inverse, des niveaux plus élevés d'IGF-1 sont corrélés à une meilleure sensibilité à l'insuline et à des niveaux de glucose sanguin plus bas. Ces découvertes suggèrent que l'IGF-1 joue un rôle crucial dans la prévention des troubles métaboliques et le maintien de l'homéostasie du glucose (Rajpathak et al., 2014).
IGF-1 et vieillissement
La voie de l'IGF-1 est hautement conservée chez diverses espèces, des invertébrés aux mammifères. Cette voie est essentielle pour réguler la croissance, le développement et la durée de vie. Chez les mammifères, la voie de l'IGF-1 implique un réseau complexe de signaux qui influencent des processus cellulaires tels que la croissance, le métabolisme et le vieillissement. L'IGF-1 exerce ses effets via le récepteur IGF-1, qui active une cascade de voies de signalisation intracellulaires favorisant la croissance et la survie des cellules (Kenyon, 2010).
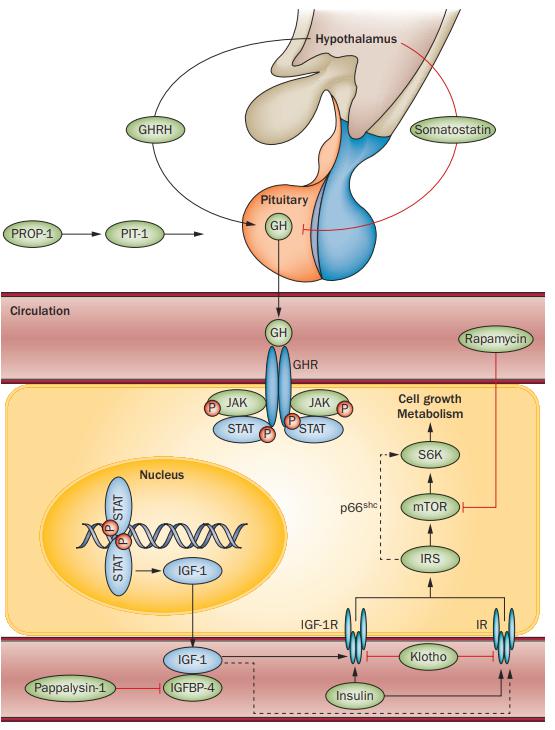
Facteurs de l'axe GH/IGF-1 connus pour influencer le vieillissement. Les gènes exprimés embryonnaires PROP1 (qui encode PROP-1) et POU1F1 (qui encode PIT-1) sont impliqués dans le développement hypophysaire, y compris la différenciation des cellules somatotropes hypophysaires.
S'il existe une voie insuline/IGF-1 chez les invertébrés, chez les vertébrés supérieurs, y compris les mammifères, cette voie se divise en deux. Ces deux voies ont des fonctions qui se chevauchent, mais l'insuline est principalement impliquée dans la régulation du métabolisme, et la voie Hormone de Croissance/IGF-1 joue un rôle important dans les processus de croissance, de développement et éventuellement d'espérance de vie. Ce sont les gènes de la cascade IGF-1 qui sont devenus les premiers "gènes du vieillissement" découverts - c'est-à-dire des gènes dont les altérations entraînaient une augmentation de l'espérance de vie.
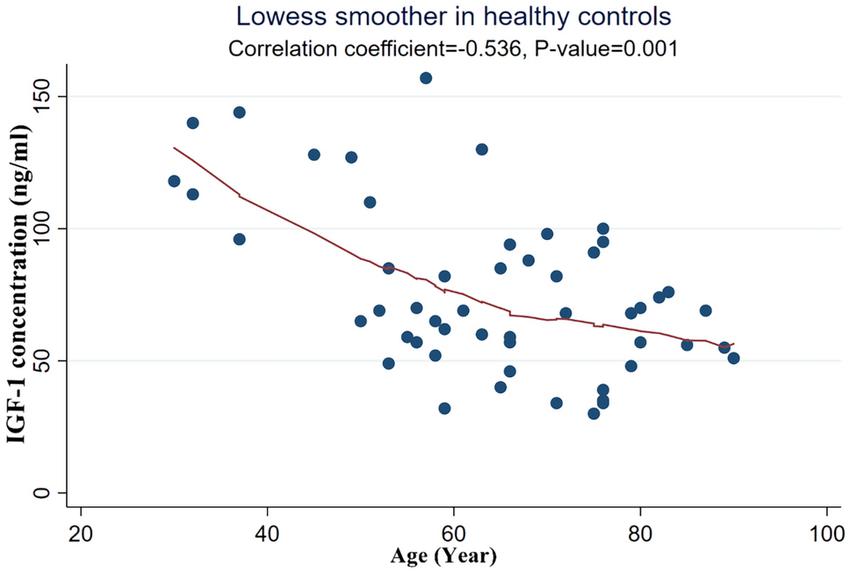
Chez l'humain, les variations des niveaux et de la signalisation de l'IGF-1 ont été liées à des maladies liées au vieillissement. De faibles niveaux d'IGF-1 sont souvent associés à un risque accru de maladies cardiovasculaires, de diabète et de troubles neurodégénératifs. À l'inverse, des niveaux plus élevés d'IGF-1 sont liés à de meilleurs résultats en matière de santé et à un risque réduit de ces conditions. Ces découvertes soulignent l'importance de l'IGF-1 dans la promotion d'un vieillissement en bonne santé et la prévention des maladies liées à l'âge (Kenyon, 2010).
Effets sur la peau
L'IGF-1 joue un rôle crucial dans le maintien de la santé de la peau et la promotion de la cicatrisation des plaies. Il agit comme un régulateur et un stimulateur de la division cellulaire dans le tissu épithélial, améliorant la croissance et le métabolisme des cellules dans les couches profondes de la peau. Cela conduit à une synthèse accélérée de collagène et à une guérison plus rapide des plaies superficielles et profondes. L'IGF-1 joue également un rôle clé dans le maintien de l'homéostasie épidermique, aidant à prévenir le vieillissement cutané et à maintenir une apparence jeune (Tavakkol et al., 1999).
Le mécanisme par lequel l'IGF-1 favorise la santé de la peau implique plusieurs processus cellulaires. Lorsque la peau est blessée, l'IGF-1 stimule la prolifération des kératinocytes, les principales cellules de l'épiderme, et des fibroblastes, les cellules responsables de la production de collagène et d'autres composants de la matrice extracellulaire. Cette augmentation de la prolifération cellulaire et de la production de matrice aide à réparer la peau endommagée et à restaurer son intégrité structurelle. De plus, l'IGF-1 améliore la migration de ces cellules vers le site de la plaie, accélérant ainsi le processus de guérison (Zhang et al., 2024).
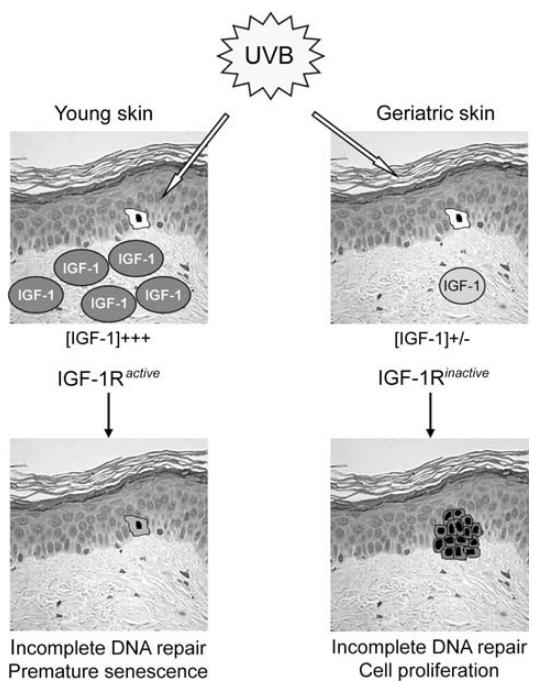
L'influence du vieillissement sur l'expression du facteur de croissance insulinomimétique 1 (IGF-1) dans la peau et son rôle dans la carcinogenèse induite par les ultraviolets-B (UVB).
Des études ont montré que l'IGF-1 peut également protéger la peau des effets du vieillissement. En favorisant la synthèse du collagène et en réduisant la dégradation des fibres de collagène, l'IGF-1 aide à maintenir l'élasticité et la fermeté de la peau. Cet effet anti-âge est particulièrement important pour prévenir la formation des rides et maintenir un teint lisse et jeune. De plus, il a été démontré que l'IGF-1 réduit l'inflammation de la peau, ce qui peut aider à prévenir les affections cutanées chroniques et améliorer la santé générale de la peau (Muraguchi et al., 2019).
Effets sur le tissu nerveux
L'IGF-1 a des effets neuroprotecteurs significatifs, améliorant la survie et la fonction des neurones. Il augmente le transport du glucose dans les neurones, leur fournissant l'énergie nécessaire à leur bon fonctionnement. Cela est particulièrement important dans des conditions de faible taux de glucose, où l'IGF-1 aide à prévenir les dommages neuronaux et la mort cellulaire. De plus, l'IGF-1 stimule la synthèse de l'ARN neuronal et favorise la formation des axones, les longues projections des neurones qui transmettent les signaux nerveux (Dyer et al., 2016).
Dans le système nerveux, l'IGF-1 améliore également la prolifération des cellules gliales, qui fournissent un soutien et une protection aux neurones. Ces cellules gliales comprennent les astrocytes, les oligodendrocytes et les microglies, jouant chacun un rôle crucial dans le maintien de la santé et du fonctionnement du système nerveux. En favorisant la prolifération et la fonction de ces cellules, l'IGF-1 aide à créer un environnement favorable aux neurones, facilitant leur croissance, leur réparation et leur survie (Carson et al., 1993).
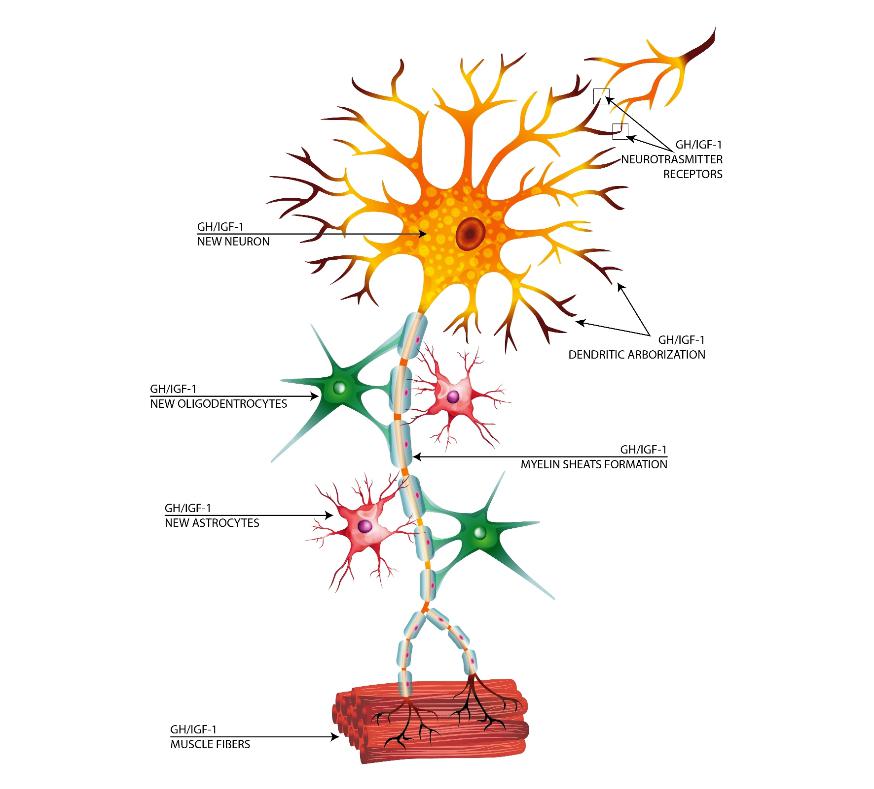
Les effets neuroprotecteurs de l'IGF-1 sont particulièrement pertinents dans les maladies neurodégénératives telles que la maladie d'Alzheimer et la maladie de Parkinson. La recherche a montré que l'IGF-1 peut réduire l'accumulation de protéines toxiques, telles que les plaques bêta-amyloïdes dans la maladie d'Alzheimer, et améliorer l'élimination de ces protéines du cerveau. Cela aide à protéger les neurones des dommages et soutient la fonction cognitive. De plus, il a été démontré que l'IGF-1 favorise la régénération des neurones endommagés, offrant des avantages thérapeutiques potentiels pour les affections neurodégénératives (Dyer et al., 2016).
Effets sur le système cardiovasculaire
L'IGF-1 joue un rôle spécialisé dans la santé cardiovasculaire en favorisant le développement et la fonction du cœur et des vaisseaux sanguins. Il améliore le débit cardiaque, le volume d'éjection, la contractilité et la fraction d'éjection, tous essentiels au maintien d'une fonction cardiaque efficace. L'IGF-1 stimule également le remodelage du tissu cardiaque, aidant à réparer les dommages après un infarctus du myocarde et à améliorer la santé cardiaque globale (Macvanin et al., 2023).
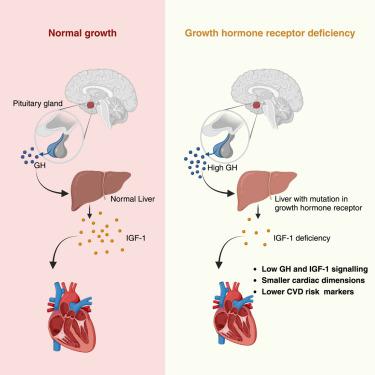
Les effets cardiovasculaires de l'IGF-1 sont médiés par plusieurs mécanismes. Tout d'abord, l'IGF-1 favorise la prolifération et la survie des cardiomyocytes, les cellules musculaires du cœur. Cela aide à maintenir l'intégrité structurelle et la fonction contractile du cœur. Deuxièmement, l'IGF-1 stimule l'angiogenèse, la formation de nouveaux vaisseaux sanguins, ce qui améliore le flux sanguin et l'apport d'oxygène au cœur et aux autres tissus. Troisièmement, l'IGF-1 a des effets anti-apoptotiques et anti-inflammatoires, réduisant la mort cellulaire et l'inflammation dans le système cardiovasculaire (De Giorgi et al., 2022).
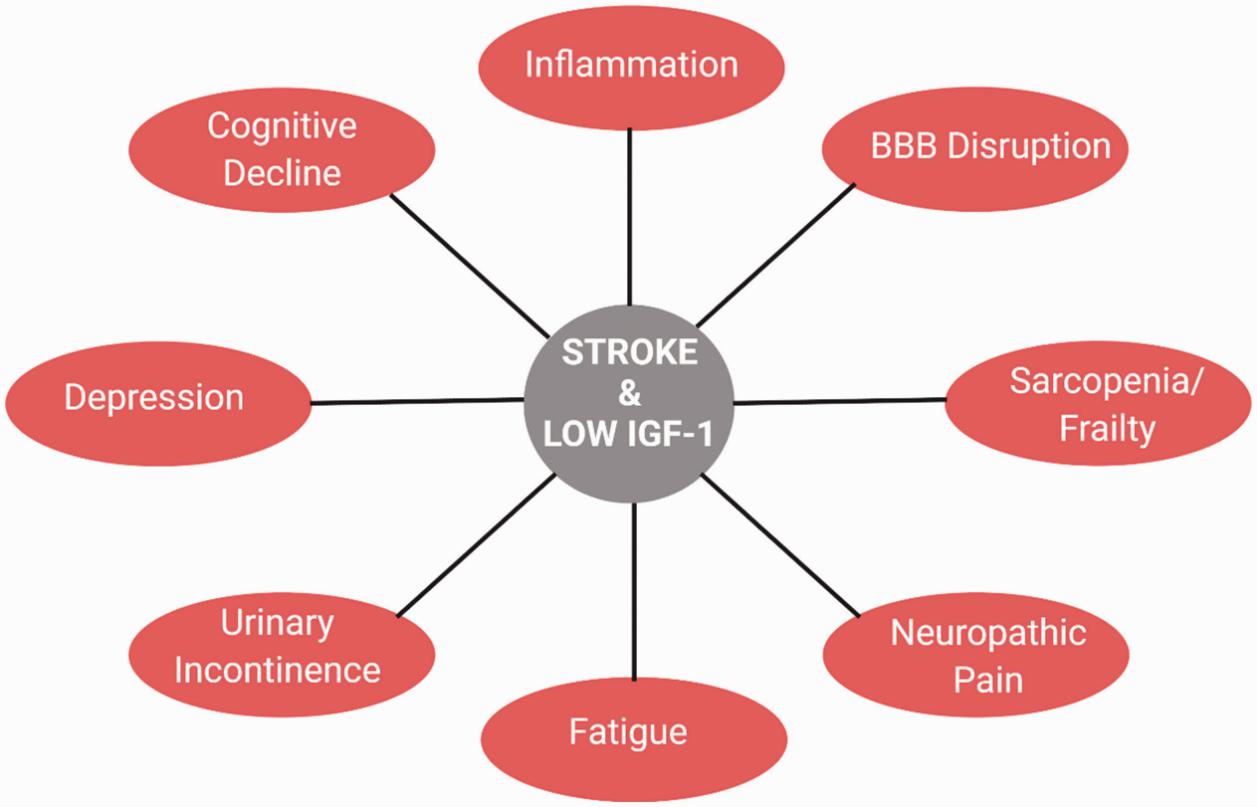
Des études cliniques ont montré que des niveaux faibles d'IGF-1 sont associés à un risque accru de maladies cardiovasculaires, y compris la maladie coronarienne et les accidents vasculaires cérébraux. Inversement, des niveaux plus élevés d'IGF-1 sont liés à une meilleure santé cardiovasculaire et à un risque réduit de ces affections. Par exemple, une étude de cohorte prospective chez des patients a révélé que les participants avec des niveaux plus élevés d'IGF-1 avaient un risque relatif de 55% inférieur d'infarctus du myocarde par rapport à ceux avec des niveaux plus faibles (Macvanin et al., 2023).
Effets sur l'immunité
L'IGF-1 a un impact significatif sur le système immunitaire, améliorant la fonction et la prolifération de diverses cellules immunitaires. Il augmente les populations de lymphocytes T, de lymphocytes B et de cellules tueuses naturelles, qui jouent toutes un rôle crucial dans la défense de l'organisme contre les infections et les maladies. L'IGF-1 améliore également l'activité des lymphocytes T, qui sont essentiels pour l'immunité à médiation cellulaire et la destruction des cellules infectées ou cancéreuses (Alpdogan et al., 2003).
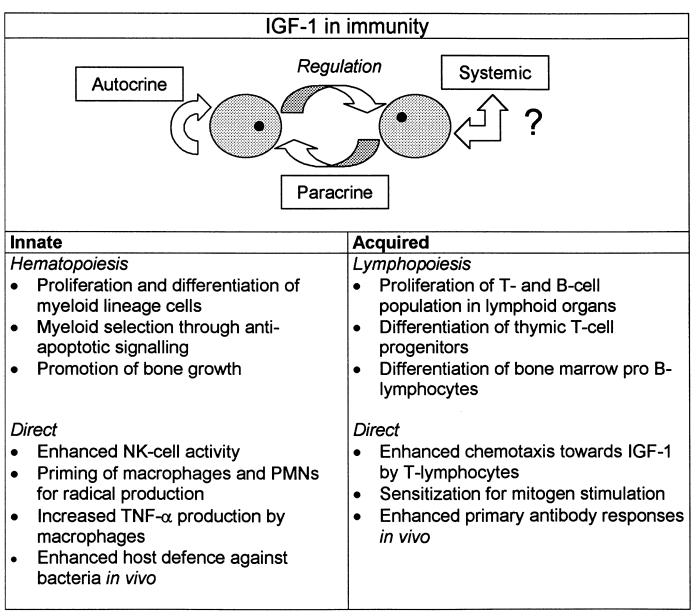
Les effets immunostimulants de l'IGF-1 sont médiés par plusieurs mécanismes. L'IGF-1 stimule la prolifération des cellules immunitaires en se liant à ses récepteurs à leur surface, entraînant une augmentation de la division et de la croissance des cellules. Cela est particulièrement important pour l'expansion des populations de cellules immunitaires en réponse aux infections ou aux défis immunologiques. De plus, l'IGF-1 améliore la fonction de ces cellules en favorisant leur activation et en augmentant leur capacité à répondre aux agents pathogènes (Dyer et al., 2016).
La recherche a montré que l'IGF-1 peut également protéger les cellules immunitaires de l'apoptose, ou mort cellulaire programmée, ce qui est crucial pour maintenir une réponse immunitaire robuste. Par exemple, des études ont démontré que l'IGF-1 peut inhiber l'apoptose des macrophages et des neutrophiles, deux types clés de cellules immunitaires impliquées dans la réponse initiale de l'organisme à l'infection. En préservant la viabilité de ces cellules, l'IGF-1 aide à assurer une réponse immunitaire efficace et soutenue (Alpdogan et al., 2003).
APPLICATION DE L'IGF-1 LR3
L'IGF-1 LR3 est souvent l'arme secrète des bodybuilders professionnels. C'est l'utilisation de ce produit qui constitue la prochaine étape de progression après les stéroïdes anabolisants et l'hormone de croissance, qui ont longtemps gagné en popularité parmi les amateurs de PEDs.
Le produit IGF-1 LR3 a un large spectre d'action et peut être utilisé à la fois pour la combustion des graisses, l'accélération de la guérison des blessures et le renforcement de l'appareil articulaire-ligamentaire, le gain de masse musculaire et la récupération accélérée après l'effort, car la substance affecte également la récupération du système nerveux. Le logiciel IGF-1 LR3 a une riche gamme de propriétés qui conviennent à de nombreux objectifs et sera un excellent complément à l'un de vos cycles, qu'il s'agisse d'un gain de masse musculaire ou d'un entraînement précompétitif.
Dosage :
Débutants : 20-40 mcg par jour
Intermédiaires : 40-60 mcg par jour
Avancés : 60-100 mcg par jour
Durée du cycle :
En général, 4-6 semaines, suivies d'une pause de durée égale pour éviter la désensibilisation.
Programme d'administration :
Fréquence : Injections quotidiennes
Moment : Administré le matin ou après l'entraînement pour maximiser l'absorption et l'efficacité.
Site d'injection : Injections sous-cutanées ou intramusculaires, avec rotation des sites pour éviter les dommages tissulaires.
Exemple
| Période (semaines) | Dosage quotidien de l'IGF-1 LR3 |
|---|---|
| 1-6 | 20-100 mcg (envisager de commencer avec une dose plus faible pour évaluer la tolérance) |
| 7-12 | Période de pause |
| 13-18 | 20-100 mcg |
| 19-24 | Période de pause |
Surdosage
Un surdosage peut entraîner les effets secondaires mentionnés ci-dessus. Le plus souvent, il s'agit d'hypoglycémie – une baisse du taux de sucre en dessous de 3,5 mmol/l. Dans ce cas, il est nécessaire de consommer une certaine quantité d'aliments glucidiques jusqu'à ce que l'état se stabilise.
Méthode d'administration
Injections intramusculaires ou sous-cutanées à l'aide de seringues à insuline.
Détection lors des tests de dopage
Si vous arrêtez de prendre le médicament trois jours avant le test, personne ne pourra détecter la substance dans le sang.
Risques potentiels
Parmi les fans de PEDs, il existe des informations qui lient l'IGF-1 au développement du cancer. Bien que cette supposée corrélation ait un grand impact sur les médias de masse, la plupart des rapports cliniques et épidémiologiques à ce jour n'ont pas révélé de relation causale entre la thérapie par l'hormone de croissance et, en conséquence, une augmentation des niveaux d'IGF-1 et un risque accru de cancer (Werner & Laron., 2020).
Sur la base de ces données, le médicament IGF-1 en lui-même ne cause pas d'oncologie, mais il a seulement une contre-indication à l'utilisation si vous avez déjà un cancer ou une prédisposition à celui-ci (marqueurs de cancer élevés). L'hormone de croissance et l'IGF-1, même à des doses pharmacologiques élevées, ne sont pas capables d'induire une transformation maligne. Cependant, l'axe GH-IGF1 est capable de "pousser" les cellules cancéreuses déjà transformées à travers les différentes phases du cycle cellulaire.
COMMENT UTILISER L'IGH-1 LR3
Toutes les hormones peptidiques de notre gamme de produits (à l'exception de l'hormone de croissance liquide) sont lyophilisées. Les peptides fournis sous forme de poudre lyophilisée sont accompagnés d'un solvant (eau bactériostatique dans une ampoule de 1 ml). Ce solvant est utilisé pour préparer une solution, qui sera ensuite conservée sous forme liquide.
Ampoule avec Solvant (Eau Bactériostatique)
Dans un environnement aqueux, les peptides se dégradent rapidement. Cela est en partie dû à la présence de bactéries, pour lesquelles l'eau constitue un environnement idéal pour la croissance et la reproduction. L'eau pour injection est stérile. Cependant, une fois l'emballage (généralement une ampoule ou un flacon) ouvert, la stérilité est compromise. Pour maintenir la stérilité le plus longtemps possible, de l'alcool benzylique ou du métacrésol est ajouté pour leurs fortes propriétés antibactériennes. Cette eau traitée est appelée bactériostatique, ce qui signifie que les bactéries restent dans un "état statique" et ne se reproduisent pas. L'hormone de croissance et d'autres peptides dans un environnement bactériostatique peuvent maintenir leur stabilité et résister à la dégradation beaucoup plus longtemps.
Comment Préparer la Solution
- Remplissez la seringue avec de l'eau. En général, le contenu du flacon est dissous dans un millilitre d'eau.
- Ajoutez de l'eau dans le flacon contenant la poudre lyophilisée. Inclinez le flacon de sorte que l'aiguille touche la paroi du flacon.
- Évitez que le diluant entre directement en contact avec la poudre lyophilisée. Le diluant doit s'écouler lentement le long des parois du flacon (ne le versez pas d'un coup et évitez de vous précipiter).
- Une fois que tout le solvant a été ajouté au flacon avec le peptide, faites tourner doucement (mais ne secouez pas) le flacon jusqu'à ce que la poudre lyophilisée se dissolve et que vous obteniez un liquide clair. La solution est maintenant prête à être utilisée.
- Conservez la solution préparée à une température de 2-8°C.
Regardez la vidéo comment préparer la solution ⤵️
https://t.me/driadaeducation/52
Seringues pour Injection
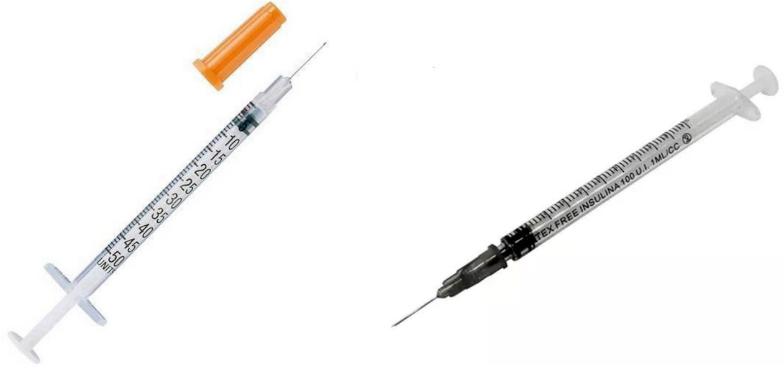
Il est recommandé d'utiliser des seringues neuves sorties de l'emballage pour éviter toute infection (la réutilisation des seringues augmente le risque d'infection). Les seringues à insuline sont généralement utilisées pour les injections sous-cutanées et peuvent avoir une aiguille amovible ou fixe. L'une des aiguilles les plus populaires pour les injections est la G30. Les seringues existent généralement en tailles de 1 ml et 0,5 ml.
Les seringues à insuline existent en formats U40 et U100, qui correspondent respectivement à un contenu en insuline de 40 unités par 1 ml et de 100 unités par 1 ml. Chaque seringue est spécifiquement conçue pour un type d'insuline particulier. Cependant, cela ne s'applique pas aux unités d'hormone de croissance ou aux mg de peptides, donc les deux types de seringues peuvent être utilisés avec des ajustements appropriés pour déterminer la bonne dose. Ces seringues ont des marquages différents, et en se référant à ces marquages, vous pouvez déterminer le nombre d'unités d'hormone de croissance à injecter. Ci-dessous, nous fournissons une image montrant le dosage de divers peptides lorsqu'ils sont mélangés avec 1 ml d'eau pour les seringues U100 et U40.

Injections Sous-Cutanées
Après dilution du peptide avec de l'eau, il est prêt à l'emploi. Tous les peptides sont injectés sous-cutanément ou par voie intramusculaire à l'aide d'une seringue à insuline.
Vous aurez besoin de :
- Tampon alcoolisé
- Seringue à insuline
- Flacon avec la solution préparée
Procédure d'Injection :
- Retirez le capuchon du flacon.
- Essuyez le bouchon en caoutchouc du flacon avec de l'alcool.
- Prenez une seringue à insuline et insérez-la dans le flacon.
- Prélevez la quantité requise de solution dans la seringue.
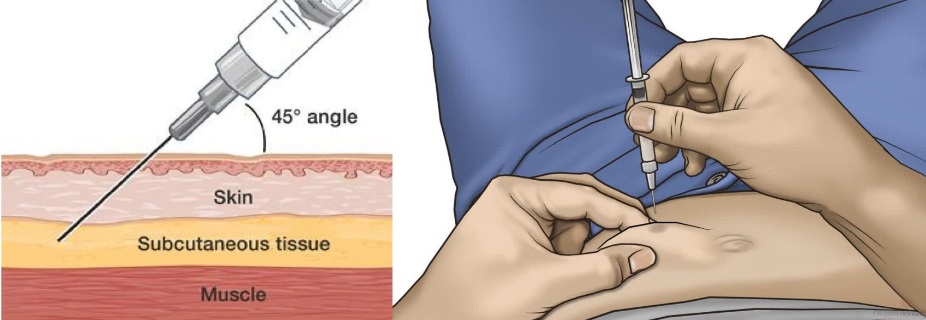
- Essuyez le site d'injection avec un tampon alcoolisé.
- Tenez l'aiguille à un angle de 30-45 degrés et injectez.
- Injectez la solution lentement.
- Après avoir terminé, maintenez l'aiguille en place pendant 10 secondes avant de la retirer pour éviter les fuites du liquide injecté.
- Augmentation synergique de la masse musculaire
- Effet synergique de la combustion des graisses
- Renforcement de l'action des stéroïdes anabolisants
- Effet synergique sur le renforcement du tissu osseux
- Augmentation synergique de la masse musculaire
- Effet synergique de la combustion des graisses
- Effet synergique sur la réparation des tendons
- Effet synergique sur le renforcement du tissu osseux
- Risque accru d'effets secondaires dus à des niveaux excessifs d'IGF-1
- Augmentation synergique de la masse musculaire
- Risque accru d'hypoglycémie
Stockage
Le stockage approprié des médicaments peptidiques est crucial pour maintenir leur efficacité. Vous trouverez ci-dessous les directives pour stocker les peptides sous différentes formes.
Stockage de la forme en poudre
La forme en poudre (non mélangée) peut être stockée à température ambiante ou au réfrigérateur. La poudre lyophilisée doit être conservée à l'abri de la lumière directe du soleil et de la chaleur excessive. Dans des conditions de stockage appropriées, les peptides sous forme sèche peuvent être conservés jusqu'à 3 ans à 2-8°C et jusqu'à 2 ans à 15-30°C. Si le flacon est endommagé et que de l'air entre à l'intérieur, la substance active se décomposera rapidement en dehors du réfrigérateur, ne conservant qu'environ la moitié de sa concentration en deux semaines. Par conséquent, si l'intégrité de l'emballage est incertaine, il est préférable de conserver le peptide au réfrigérateur.
Stockage de l'eau bactériostatique
L'eau bactériostatique doit toujours être conservée au réfrigérateur à 2-8°C pour maintenir ses propriétés. Si le peptide et l'eau bactériostatique sont stockés ensemble, conservez l'ensemble au réfrigérateur.
Stockage de la solution
Après avoir mélangé la poudre avec l'eau de l'ampoule, la solution peptidique doit être conservée au réfrigérateur. Sans réfrigération, le peptide commence à se dégrader, et en quelques jours, les molécules se désagrégeront complètement. La durée de conservation de chaque peptide varie. Par exemple, l'hormone de croissance peut être conservée au réfrigérateur pendant seulement 2-3 jours, tandis que l'HCG peut durer environ 5 semaines. En moyenne, d'autres peptides peuvent être conservés au moins 30 jours, bien que certains puissent durer encore plus longtemps. Le taux de dégradation dépend également du nombre de bactéries introduites lors de la perforation du flacon, ce qui est inévitable dans une certaine mesure.
!!! NE JAMAIS STOCKER LES PEPTIDES AU CONGÉLATEUR !!!
Utilisation avec des stéroïdes anabolisants
Il est également parfaitement approprié d'utiliser l'IGF-1 avec des stéroïdes anabolisants et d'autres médicaments ayant des effets similaires. L'IGF-1-1 renforce les effets des stéroïdes anabolisants en augmentant le nombre de récepteurs aux androgènes. Le médicament IGF-1 est un anabolisant extrêmement puissant qui, en combinaison avec les stéroïdes, entraîne une augmentation très importante de la masse musculaire maigre. En même temps, l'IGF-1 possède de nombreuses autres propriétés utiles qui créent ensemble les conditions maximales pour la croissance.
Tous les stéroïdes anabolisants agissent sur les muscles à travers des structures spéciales – les récepteurs. On pense que si vous utilisez des stéroïdes pendant longtemps, le nombre de ces récepteurs diminue. Le nombre de ces récepteurs diminue également avec l'âge. Dans ce cas, il devient nécessaire d'utiliser de fortes doses de stéroïdes. À 20 ans, 300 mg de propionate de testostérone agissent plus puissamment qu'à 30 ans. À 30 ans, 600 mg sont nécessaires pour obtenir le même effet. L'IGF-1 active les cellules et augmente le nombre de récepteurs aux androgènes, et à 30 ans, 300 mg de propionate de testostérone agiront de la même manière qu'à 20 ans.
Effets
Utilisation avec l'hormone de croissance (Somatropin)
L'utilisation de la somatotropine en même temps peut être recommandée, bien que cela puisse ne pas sembler logique à première vue, néanmoins, de nombreux culturistes professionnels le font. Lorsqu'ils sont utilisés ensemble, leurs effets se cumulent – comme un effet anabolique pour la croissance musculaire, ainsi que pour la réparation et la régénération des cartilages et autres structures de collagène. De plus, l'hormone de croissance et l'IGF-1 augmenteront ensemble la combustion des graisses.
Il convient de noter qu'en plus des effets bénéfiques, la présence d'effets secondaires peut également survenir. Il faut comprendre que le niveau d'IGF lors de l'utilisation des deux médicaments augmentera considérablement, il ne faut donc pas prolonger cette utilisation.
Effets
Utilisation avec l'insuline
Comme le nom IGF-1 l'indique, il a une structure similaire à l'insuline, et se lie non seulement à son propre récepteur IGF1R, mais aussi au récepteur de l'insuline — et vice versa. Cependant, l'affinité de liaison pour l'IGF1R et le récepteur de l'insuline est différente, avec une affinité élevée de l'IGF-1 pour l'IGF1R et environ 10 fois moins d'affinité pour le récepteur de l'insuline.
D'autre part, l'affinité de l'insuline pour son propre récepteur est environ 100 fois plus élevée que pour l'IGF1R. De plus, malgré la similitude de structure, l'IGF-1 et l'insuline montrent une répartition différente dans les tissus, une cinétique d'internalisation différente et une répartition sous-cellulaire différente des récepteurs hormonaux. Par conséquent, les deux hormones peuvent affecter des voies similaires, mais à des degrés différents, et, en outre, activer différemment d'autres voies situées en aval.
Ces hormones peuvent être comparées en ce qui concerne l'effet sur le métabolisme du glucose dans le corps. Lorsqu'elles sont utilisées ensemble, un effet secondaire tel que l'hypoglycémie (chute du taux de sucre) sera si prononcé qu'il créera des risques pour la vie.